Амфотерные металлы список
Свойства амфотерных металлов
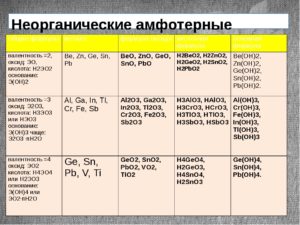
Амфотерные металлы представлены не сложными элементами, являющимися неким аналогом группы компонентов металлического типа. Сходство прослеживается в ряде свойств физического и химического направления. Причем, за самими веществами не замечено способности к свойствам амфотерного типа, а различные соединения вполне способны к их проявлению.
Для примера можно рассмотреть гидроксиды с оксидами. У них явно прослеживается двойственная химическая природа. Она выражена в том, что, в зависимости от условий, выше названные соединения могут обладать свойствами либо щелочей, либо кислот.
Понятие амфотерности появилось достаточно давно, оно знакомо науке еще с 1814 года. Термин «амфотерность» выражал способность химического вещества вести себя определенным образом при проведении кислотной (главной) реакции.
Получаемые свойства зависят от того, каков тип самих присутсвующих реагентов, вида растворителя и условий, при которых проводится реакция.
Что представляют собой амфотерные металлы?
Список амфотерных металлов включает в себя множество наименований. Некоторые из них можно с уверенность назвать амфотерными, некоторые – предположительно, иные – условно. Если рассматривать вопрос масштабно, то для краткости можно назвать просто порядковые номера выше указанных металлов.
Эти номера: 4,13, с 22 до 32, с 40 до 51, с 72 до 84, со 104 до 109. Но есть металлы, которые вправе назваться основными. К ним относятся хром, железо, алюминий и цинк. Дополняют основную группу стронций и бериллий. Самым распространенным из всех перечисленных на данный момент является алюминий.
Именно его сплавы уже много столетий используются в самых разнообразных сферах и областях применения. Металл имеет отличную антикоррозийную стойкость, легко поддается литью и различным типам механической обработки.
Кроме того, популярность алюминия дополняется такими преимуществами, как высокая теплопроводность и хорошая электропроводность.Алюминий — амфотерный металл, для которого свойственно проявлять химическую активность. Стойкость данного металла определяется прочной оксидной пленкой и, в обычных условиях окружающей среды, при реакциях химического направления, алюминий выступает восстановительным элементом.
Такое амфотерное вещество способно взаимодействовать с кислородом, в случае раздробления металла на мелкие частицы. Для такого взаимодействия необходимо влияние высокого температурного режима. Химическая реакция при соприкосновении с кислородной массой сопровождается огромным выделением тепловой энергии.
При температуре свыше 200 градусов взаимодействие реакций при соединении с таким веществом, как сера, образовывает сульфид алюминия.
Амфотерный алюминий не способен напрямую взаимодействовать с водородом, а при смешивании этого металла с другими металлическими компонентами возникают различные сплавы, содержащие соединения интерметаллического типа.
Железо — амфотерный металл, который является одной из побочных подгрупп группы 4 периода в системе элементов химического типа. Данный элемент выделяется как самое распространенное составляющее группы металлических веществ, в составе компонентов земной коры.
Железо классифицируется как простое вещество, среди отличительных свойств которого можно выделить его ковкость, серебристо-белую цветовую гамму.
Такой металл обладает способностью провоцировать возникновение повышенной химической реакции и быстро переходит в стадию корродирования при воздействии высокой температуры.Помещенное в чистый кислород железо полностью перегорает, а доведенное до мелкодисперсного состояния может самовоспламеняться на простом воздухе. Находясь на воздухе металлическое вещество быстро окисляется вследствие чрезмерной влажности, то есть, ржавеет. При горении в кислородной массе образуется своеобразная окалина, которая называется оксидом железа.
Основные свойства амфотерных металлов
Свойства амфотерных металлов — основное понятие в амфотерности. Рассмотрим, что же они из себя представляют. В стандартном состоянии каждый металлов является твердым телом. Поэтому их принято считать слабыми электролитами.
Кроме того, ни один металл не может растворяться в воде. Основания получаются путем специальной реакции. В ходе этой реакции соль металла соединяется с небольшой дозой щелочи.
Правила требуют проводить весь процесс аккуратно, осторожно и довольно медленно.
При соединении амфотерных веществ с кислотными оксидами или непосредственно кислотами, первые выдают реакцию, свойственную основаниям. Если же такие основания соединять с основаниями, проявляются свойства кислот.
Сильное нагревание амфотерных гидроксидов приводит к их распаду. В результате распада образуется вода и соответствующий амфотерный оксид.
Как видно из наведенных примеров, свойства достаточно обширны и требуют тщательного анализа, который можно провести в ходе химических реакций.
Химические свойства амфотерных металлов можно сравнить со свойствами обычных металлов, чтобы провести параллель или увидеть разницу. У всех металлов достаточно низкий потенциал ионизации, благодаря чему в химических реакциях они выступают в роли восстановителей. Стоит отметить также, что электроотрицательность неметаллов выше, чем данный показатель у металлов.
Амфотерные металлы проявляют как восстановительные, так и окислительные свойства. Но при этом у амфотерных металлов имеются соединения, характеризующиеся отрицательной степенью окисления. Всем металлам свойственна возможность образования основных гидроксидов и оксидов.
Зависимо от роста порядкового номера в периодическом ранжире замечено убывание основности металла. Следует также заметить, что металлы, в основной своей части, могут окисляться только определенными кислотами. Так, взаимодействие с азотной кислотой у металлов происходит по-разному.
Металлы неметаллы амфотерные, которые являются простыми веществами, имеют явное различие по своему строению и индивидуальным особенностям относительно физических и химических проявлений. Тип некоторых из данных веществ легко определить визуальным способом. Например, медь является простым амфотерным металлом, а бром классифицируется как неметалл.
Чтобы не ошибиться в определении разновидности простых веществ необходимо четко знать все признаки, которые отличают металлы от неметаллов. Основным различием металлов и неметаллов выступает способность первых отдавать электроны, расположенные во внешнем энергетическом секторе.
Неметаллы наоборот, притягивают электроны в зону внешнего накопителя энергетики.
Все металлы имеют свойство передавать энергетический блеск, что делает их хорошими проводниками тепловой и электрической энергии, а неметаллы невозможно использовать в качестве пропускника электричества и тепла.| Температура изгтотовления различных конструкций из алюминиевых сплавов, как правило, не превышает 350 градусов. Это обусловлено свойствами алюминия — при длительной выдержке таких сплавов, как авиаль или… |
| Основным составным веществом алюминевого сплава является, как становится ясно из названия, алюминий. К другим, наиболее распространенным элементами, которые входят в состав сплавов на основе алюминия, можно отнести медь, железо, цинк… |
| Щелочноземельные металлы представлены рядом элементов, которые относятся ко II группе периодической системы Менделеева. Такое название вещества получили благоларя тому, что результатом их взаимодействия с водой является образование щелочной среды. Если рассматривать физические свойства… |
| В результате применения различных обработок свойства стали могут меняться. Благодаря полиморфмизму, который способствует изменению кристаллической решетки материала в процессе нагревания или охлаждения, получение необходимой струтуры стали становится… |
| Необходимость идентификации сталей и сплавов была обусловлена их значичтельным количеством, однако даже на сегодняшний день производители металлопроката не могут предоставить единую систему марок сталей, что порождает ряд трудностей для… |
| Изготавливают жаропрочные стали и сплавы на основе железа, добавляя и другие мтеаллы. К примеру, благодаря наличию в составе хрома и никеля материал способен противостоять воздействию высоких температур. Если рассматривать процентное соотношение… |
Амфотерные металлы список — Справочник металлиста

ХромАмфотерный хром
Простые вещества сходные с металлическими элементами по структуре и ряду химических и физических параметров называют амфотерными, т.е. это те элементы, проявляющие химическую двойственность.
Надо отметить, что это не сами металли, а их соли или оксиды.
К, примеру, оксиды некоторых металлов могут обладать двумя свойствами, при одних условиях они могут проявлять свойства присущие кислотам, в других, они ведут себя как щелочи.
К основным амфотерным металлам относят алюминий, цинк, хром и некоторые другие.
Термин амфотерность был введен в оборот в начале XIX века. В то время химические вещества разделяли на основании их сходных свойств, проявляющиеся при химических реакциях.
Что такое амфотерные металлы
Список металлов, которые можно отнести амфотерным, достаточно велик. Причем некоторые из них можно назвать амфотерными, а некоторые – условно.
Перечислим порядковые номера веществ, под которыми они расположены в Таблице Менделеева. В список входят группы с 22 по 32, с 40 по 51 и еще много других. Например, хром, железо и ряд других можно с полным основанием называть основными, к последним можно отнести и стронций с бериллием.
Кстати, самым ярким представителем амфорных металлов считают алюминий.
Именно его сплавы в течение длительного времени используют практически во всех отраслях промышленности. Из него делают элементы фюзеляжей летательных аппаратов, кузовов автомобильного транспорта, и кухонную посуду.
Он стал незаменим в электротехнической промышленности и при производстве оборудования для тепловых сетей. В отличии от многих других металлов алюминий постоянно проявляет химическую активность. Оксидная пленка, которая покрывает поверхность металла, противостоит окислительным процессам.
В обычных условиях, и в некоторых типах химических реакций алюминий может выступать в качестве восстановительного элемента.
Этот металл способен взаимодействовать с кислородом, если его раздробить на множество мелких частиц. Для проведения операции такого рода необходимо использование высокой температуры. Реакция сопровождается выделением большого количества тепловой энергии.
При повышении температуры в 200 ºC, алюминий вступает в реакцию с серой. Все дело в том, что алюминий, не всегда, в нормальных условиях, может вступать в реакцию с водородом. Между тем, при его смешивании с другими металлами могут возникать разные сплавы.
Еще один ярко выраженный металл, относящийся к амфотерным – это железо. Этот элемент имеет номер 26 и расположен между кобальтом и марганцем. Железо, самый распространенный элемент, находящийся в земной коре.Железо можно классифицировать как простой элемент, имеющий серебристо-белый цвет и отличается ковкостью, разумеется, при воздействии высоких температур. Может быстро начинать коррозировать под воздействием высоких температур.
Железо, если поместить его в чистый кислород полностью прогорает и может воспламениться на открытом воздухе.
Такой металл обладает способностью быстро переходить в стадию корродирования при воздействии высокой температуры. Помещенное в чистый кислород железо полностью перегорает. Находясь на воздухе металлическое вещество, быстро окисляется вследствие чрезмерной влажности, то есть, ржавеет. При горении в кислородной массе образуется своеобразная окалина, которая называется оксидом железа.
Свойства амфотерных металлов
Они определены самим понятием амфотерности. В типовом состоянии, то есть обычной температуре и влажности, большая часть металлов представляет собой твердые тела. Ни один металл не подлежит растворению в воде.
Щелочные основания проявляются только после определенных химических реакций. В процессе прохождения реакции соли металла вступают во взаимодействие.
Надо отметить что правила безопасности требуют особой осторожности при проведении этой реакции.
Соединение амфотерных веществ с оксидами или самими кислотами первые показывают реакцию, которая присуща основаниями. В тоже время если их соединять с основаниями, то будут проявляться кислотные свойства.
Нагрев амфотерных гидроксидов вынуждает их распадаться на воду и оксид. Другими словами свойства амфотерных веществ весьма широки и требуют тщательного изучения, которое можно выполнить во время химической реакции.
Свойства амфотерных элементов можно понять, сравнив их с параметрами традиционных материалов. Например, большинство металлов имеют малый потенциал ионизации и это позволяет им выступать в ходе химических процессов восстановителями.
Амфотерные — могут показать как восстановительные, так и окислительные характеристики. Однако, существуют соединения которые характеризуются отрицательным уровнем окисления.
Абсолютно все известные металлы имеют возможность образовывать гидроксиды и оксиды.
Всем металлам свойственна возможность образования основных гидроксидов и оксидов. Кстати, металлы могут вступать в реакцию окисления только с некоторыми кислотами. Например, реакция с азотной кислотой может протекать по-разному.
Конспект

Ключевые слова конспекта: амфотерность, амфотерные оксиды, амфотерные гидроксиды,
Гидроксиды – это неорганические соединения, образованные тем или иным элементом, кислородом и водородом.
В гидроксидах обязательно имеется водород, связанный с кислородом (связь О–Н). В некоторых гидроксидах водород может непосредственно соединяться с атомами элемента.
Например, в H3РO3 два атома водорода связаны с атомами кислорода, а один – с атомом фосфора.
В ряде случаев гидроксиды являются продуктами гидратации (соединения с водой) соответствующих оксидов, хотя многие оксиды непосредственно с водой не взаимодействуют. В результате дегидратации гидроксидов образуются соответствующие оксиды.
Гидроксиды могут быть основными (основания), кислотными (кислородсодержащие кислоты) и амфотерными. Примерами основных гидроксидов являются NaOH, Ва(ОН)2, Mg(OH)2. Примерами кислотных гидроксидов являются НСlO4 (хлорная кислота, высший гидроксид хлора), H3РO4 (ортофосфорная кислота, высший гидроксид фосфора), H2SO4 (серная кислота, высший гидроксид серы).
Графические формулы перечисленных гидроксидов приведены ниже. Во всех гидроксидах имеется связь О–Н:
ПОНЯТИЕ ОБ АМФОТЕРНЫХ ОКСИДАХ И ГИДРОКСИДАХ
Амфотерность (от греч. amphoteros – и тот, и другой) – способность химических соединений проявлять и кислотные, и основные свойства в зависимости от природы реагента, с которым амфотерное вещество вступает в кислотно-основное взаимодействие.
Амфотерные оксиды и гидроксиды – оксиды и гидроксиды, проявляющие как основные, так и кислотные свойства. Они реагируют как с кислотами, так и с основаниями. Амфотерным оксидам соответствуют амфотерные гидроксиды, например: ВeО – Вe(ОН)2, Сr2O3 – Сr(ОН)3.
Амфотерные гидроксиды практически нерастворимы в воде. Их основные и кислотные свойства выражены слабо, они являются слабыми кислотами и слабыми основаниями.
Амфотерными оксидами и гидроксидами являются, как правило, оксиды и гидроксиды металлов, в которых степень окисления металла +3, +4, иногда +2.
Среди оксидов элементов главных подгрупп амфотерными являются: BeO, Al2O3, SnO, SnO2, PbO, Sb2O3.
Амфотерными гидроксидами являются следующие гидроксиды элементов главных подгрупп: Ве(ОН)2, Al(ОН)3, Рb(ОН)2 и некоторые другие.Оксиды и гидроксиды элементов побочных подгрупп, соответствующие высоким степеням окисления, как правило, являются кислотными, например: СrO3 (ему соответствует H2СrO4), Мn2O7 (ему соответствует НМnO4).
Для низших оксидов и гидроксидов характерно преобладание основных свойств, например: СrO и Сr(ОН)2, МnО и Мn(ОН)2.
Оксиды и гидроксиды, в которых степени окисления элементов +3 и +4, являются, как правило, амфотерными: Сг2O3 и Cr(OH)3, Fe2O3 и Fe(OH)3. Однако последние элементы в декадах d–элементов (например, Zn) образуют амфотерные оксиды и гидроксиды даже в низких степенях окисления, например ZnO и Zn(OH)2.
ХИМИЧЕСКИЕ СВОЙСТВА АМФОТЕРНЫХ ОКСИДОВ И ГИДРОКСИДОВ
Рассмотрим амфотерные свойства оксида и гидроксида цинка – ZnO и Zn(OH)2. Оба вещества реагируют с кислотами:
ZnO + 2HNO3 = Zn(NO3)2 + H2O
Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O
Оксид и гидроксид цинка реагируют также и со щелочами:
В результате реакций со щелочами в растворах образуются комплексные ионы – тетрагидроксоцинкаты (например, Na2[Zn(OH)4]), а при сплавлении – цинкаты (например, Na2ZnO2). Чтобы составить формулы цинкатов, запишите формулу гидроксида цинка Zn(OH)2 как формулу кислоты – H2ZnO2. Кислотным остатком такой кислоты является ион ZnO22–.
При диссоциации этих солей в растворах образуются ионы, в которых цинк входит в состав анионов, поэтому говорят, что в этих соединениях «цинк в анионной форме».
Докажем амфотерность оксида и гидроксида алюминия Al(ОН)3. Он растворяется в кислотах с образованием солей, где алюминий находится в катионной форме:
Al(ОН)3 + 3Н+ = Al3+ + 3H2O
Но гидроксид алюминия взаимодействует и со щелочами. При сплавлении со щелочами образуются алюминаты (метаалюминаты):
Al(ОН)3 + NaOH = NaAlO2 + 2H2O
Чтобы составить формулы алюминатов, запишите формулу гидроксида алюминия Al(ОН)3 как H3AlO3. Теперь представьте, что от 1 моль этого соединения отщепляется 1 моль воды. Образуется соединение НАlO2, в котором кислотным остатком будет ион AlO2–.
В образовавшейся соли алюминий образует анион AlO2– (алюминий в анионной форме). В растворах в результате реакции со щёлочью образуется комплексный тетрагидроксоалюминат-ион [Al(ОН)4]–:
Al(ОН)3 + NaOH = Na[Al(OH)4] (тетрагидроксоалюминат натрия)
Некоторые амфотерные оксиды и гидроксиды не проявляют амфотерность в обычных условиях и в растворах ведут себя как основные. Амфотерность таких соединений проявляется в более жёстких условиях. Например, гидроксид железа (III) Fe(OH)3 легко реагирует с кислотами:Fe(OH)3 + 3НCl = FeCl3 + 3H2O
Fe(OH)3 + NaOH = NaFeO2 + 2H2O
Признаком этой реакции будет растворение бурого осадка. А вот при добавлении раствора щёлочи гидроксид железа (III) не растворяется. Тогда, может быть, считать его основанием, не растворимым в воде? Дело в том, что в данном случае соль образуется при плавлении со щёлочью.
Естественно, что в ходе плавления происходит разложение гидроксида на оксид и воду, и в действительности реакция идёт между оксидом и щёлочью:
Fe2O3 + 2NaOH = 2NaFeO2 + H2O
Таким образом, гидроксид железа (III) можно отнести к амфотерным гидроксидам, хотя основные свойства у него преобладают.
Конспект урока «Амфотерные оксиды и гидроксиды».
Следующая тема: «».
Амфотерные металлы в таблице менделеева

Свойства химических элементов позволяют объединять их в соответствующие группы. На этом принципе была создана периодическая система, изменившая представление о существующих веществах и позволившая предположить существование новых, ранее неизвестных элементов.
Периодическая система Менделеева
Периодическая таблица химических элементов была составлена Д. И. Менделеевым во второй половине XIX века. Что такое это, и для чего она нужна? Она объединяет все химические элементы по возрастанию атомного веса, причем, все они расставлены так, что их свойства изменяются периодическим образом.
Периодическая система Менделеева в химии свела в единую систему все существующие элементы, прежде считавшиеся просто отдельными веществами.
На основании ее изучения были предсказаны, а впоследствии — синтезированы новые химические вещества. Значение этого открытия для науки невозможно переоценить, оно значительно опередило свое время и дало толчок к развитию химии на многие десятилетия.
Существует три наиболее распространенных варианта таблицы, которые условно именуются «короткая», «длинная» и «сверхдлинная». Основной считается длинная таблица, она утверждена официально. Отличием между ними является компоновка элементов и длина периодов.
Что такое период
Система содержит 7 периодов. Они представлены графически в виде горизонтальных строк. При этом, период может иметь одну или две строки, называемые рядами. Каждый последующий элемент отличается от предыдущего возрастанием заряда ядра (количества электронов) на единицу.
Если не усложнять, период — это горизонтальная строка периодической таблицы. Каждый из них начинается металлом и заканчивается инертным газом.
Собственно, это и создает периодичность — свойства элементов изменяются внутри одного периода, вновь повторяясь в следующем.
Первый, второй и третий периоды — неполные, они называются малыми и содержат соответственно 2, 8 и 8 элементов. Остальные — полные, они имеют по 18 элементов.
Что такое группа
Группа — это вертикальный столбец, содержащий элементы с одинаковым электронным строением или, говоря проще, с одинаковой высшей валентностью. Официально утвержденная длинная таблица содержит 18 групп, которые начинаются со щелочных металлов и заканчиваются инертными газами.
Каждая группа имеет свое название, облегчающее поиск или классификацию элементов. Усиливаются металлические свойства в независимости от элемента по направлению сверху-вниз. Это связано с увеличением количества атомных орбит — чем их больше, тем слабее электронные связи, что делает более ярко выраженной кристаллическую решетку.
Металлы в периодической таблице
Металлы в таблице Менделеева имеют преобладающее количество, список их достаточно обширен. Они характеризуются общими признаками, по свойствам они неоднородны и делятся на группы.
Некоторые из них имеют мало общего с металлами в физическом смысле, а иные могут существовать только доли секунды и в природе абсолютно не встречаются (по крайней мере, на планете Земля), поскольку созданы, точнее, вычислены и подтверждены в лабораторных условиях, искусственно.
Каждая группа имеет собственные признаки, название и довольно заметно отличается от других. Особенно это различие выражено у первой группы.
Положение металлов
Какого положение металлов в периодической системе? Элементы расположены по увеличению атомной массы или количества электронов и протонов. Их свойства изменяются периодически, поэтому аккуратного размещения по принципу «один к одному» в таблице нет.
Как определить металлы, и возможно ли это сделать по таблице Менделеева? Для того, чтобы упростить вопрос, придуман специальный прием: условно по местам соединения элементов проводится диагональная линия от Бора до Полония (или до Астата). Те, что оказываются слева — металлы, справа — неметаллы.
Это было бы очень просто и здорово, но есть исключения — Германий и Сурьма.
Важно! Это работает только в длинной системе, на коротком варианте таблицы Менделеева многие металлы оказываются справа.
Такая «методика» — своего рода шпаргалка, она придумана лишь для упрощения процесса запоминания. Для более точного представления следует запомнить, что список неметаллов составляет всего 22 элемента, поэтому отвечая на вопрос, сколько всего металлов всего содержится в таблице Менделеева
На рисунке можно наглядно увидеть, какие элементы являются неметаллами и как они располагаются в таблице по группам и периодам.
! Каково содержание кислорода в воздухе: процентный состав и норма
Общие физические свойства
Существуют общие физические свойства металлов. К ним относятся:
- Пластичность.
- Характерный блеск.
- Электропроводность.
- Высокая теплопроводность.
- Все, кроме ртути, находятся в твердом состоянии.
Следует понимать, что свойства металлов очень различаются относительно их химической или физической сути. Некоторые из них мало похожи на металлы в обыденном понимании этого термина. Например, ртуть занимает особенное положение.
Она при обычных условиях находится в жидком состоянии, не имеет кристаллической решетки, наличию которой обязаны своими свойствами другие металлы.
Свойства последних в этом случае условны, с ними ртуть роднят в большей степени химические характеристики.
Интересно! Элементы первой группы, щелочные металлы, в чистом виде не встречаются, находясь в составе различных соединений.
Самый мягкий металл, существующий в природе — цезий — относится к этой группе. Он, как и другие щелочные подобные вещества, мало общего имеет с более типичными металлами.Некоторые источники утверждают, что на самом деле, самый мягкий металл калий, что сложно оспорить или подтвердить, поскольку ни тот, ни другой элемент не существует сам по себе — будучи выделенным в результате химической реакци они быстро окисляются или вступают в реакцию.
Вторая группа металлов — щелочноземельные — намного ближе к основным группам. Название «щелочноземельные» происходит из древних времен, когда окислы назывались «землями», поскольку они имеют рыхлую рассыпчатую структуру.
Более-менее привычными (в обиходном смысле) свойствами обладают металлы начиная с 3 группы. С увеличением номера группы количество металлов убывает, замещаясь неметаллическими элементами.
Последняя группа состоит из инертных (или благородных) газов.
Определение металлов и неметаллов в таблице Менделеева. Простые и сложные вещества.
Простые вещества (металлы и неметаллы)
Вывод
Соотношение металлов и неметаллов в таблице Менделеева явно перевешивает в пользу первых. Такое положение свидетельствует о том, что группа металлов объединена слишком широко и требует более подробной классификации, что признается научным сообществом.
! Основной закон Гесса и следствия из него
Амфотерность
Амфотерность (от др.-греч. амфотеро — «двойственный»,«обоюдный») — способность некоторых соединений проявлять в зависимости отусловий как кислотные, так и основные свойства.
Понятие амфотерность как характеристикадвойственного поведения вещества было введено в 1814 г. Ж. Гей-Люссаком и Л.Тенаром.
Амфотерными называютсяоксиды и гидроксиды, которые проявляют и основные и кислотные свойства взависимости от условий.
Наиболеечасто встречающиеся амфотерные оксиды (и соответствующие им гидроксиды):
ZnO,Zn(OH)2, BeO, Be(OH)2, PbO, Pb(OH)2, SnO,Sn(OH)2, Al2O3, Al(OH)3, Fe2O3,Fe(OH)3, Cr2O3, Cr(OH)3
Свойства амфотерных соединенийзапомнить не сложно: они взаимодействуют с
ОСНОВНЫЕ СВОЙСТВА
Оксиды:
Al2O3 + 6HCl =2AlCl3 + 3H2O;
ZnO + H2SO4 = ZnSO4 +H2O;
BeO + HNO3 = Be(NO3)2 +H2O
Гидроксиды:
Fe(OH)3 + 3HCl = FeCl3 +3H2O;
Pb(OH)2 + 2HCl = PbCl2 +2H2O
Сложней для понимания реакция со щелочью. Рассмотрим на примере взаимодействия гидроксида цинка с гидроксидом калия при сплавлении.
Амфотерные соединения взаимодействуя с основаниями, ведут себя как кислоты. Вот и запишем гидроксидцинка Zn(OH)2 каккислоту. У кислоты водород спереди, вынесем его: H2ZnO2.
И реакция щелочи с гидроксидом будет протекать как будто он –кислота. «Кислотный остаток» ZnO22- двухвалентный:
2KOH(тв.) + H2ZnO2(тв.) = K2ZnO2 + 2H2O
Полученноевещество K2ZnO2 называется метацинкат калия (или простоцинкат калия). Это вещество – соль калия и гипотетической «цинковой кислоты» H2ZnO2 (солями такие соединения называть не совсем правильно, нодля собственного удобства мы про это забудем).
Гидроксид цинка записывать в виде H2ZnO2 не принято. Пишем как обычно Zn(OH)2,но подразумеваем (для собственного удобства), что это кислота H2ZnO2:
Амфотерные металлы

Простые вещества сходные с металлическими элементами по структуре и ряду химических и физических параметров называют амфотерными, т.е. это те элементы, проявляющие химическую двойственность.
Надо отметить, что это не сами металли, а их соли или оксиды.
К, примеру, оксиды некоторых металлов могут обладать двумя свойствами, при одних условиях они могут проявлять свойства присущие кислотам, в других, они ведут себя как щелочи.
К основным амфотерным металлам относят алюминий, цинк, хром и некоторые другие.
Термин амфотерность был введен в оборот в начале XIX века. В то время химические вещества разделяли на основании их сходных свойств, проявляющиеся при химических реакциях.
Как отличить металл от неметалла
Главное различие заключается в том, что металлы отдают электроны, которые находятся во внешнем электронном облаке. Неметаллы, активно их притягивают.
Все металлы являются хорошими проводниками тепла и электричества, неметаллы, такой возможности лишены.
Основания амфотерных металлов
В нормальных условиях это вещества не растворяются в воде и их можно спокойно отнести к слабым электролитам. Такие вещества получают после проведения реакции солей металла и щелочи. Эти реакции довольно опасны для тех, кто их производит и поэтому, например, для получения гидроксида цинка в емкость с хлоридом цинка медленно и аккуратно, по капле надо вводить едкий натр.
Вместе тем, амфотерные — взаимодействуют с кислотами как основания. То есть при выполнении реакции между соляной кислотой и гидроксидом цинка, появится хлорид цинка. А при взаимодействии с основаниями, они ведут себя как кислоты.
Амфотерность

Амфотерность (от др.-греч. амфотеро — «двойственный»,«обоюдный») — способность некоторых соединений проявлять в зависимости отусловий как кислотные, так и основные свойства.
Понятие амфотерность как характеристикадвойственного поведения вещества было введено в 1814 г. Ж. Гей-Люссаком и Л.Тенаром.
Амфотерными называютсяоксиды и гидроксиды, которые проявляют и основные и кислотные свойства взависимости от условий.
Наиболеечасто встречающиеся амфотерные оксиды (и соответствующие им гидроксиды):
ZnO,Zn(OH)2, BeO, Be(OH)2, PbO, Pb(OH)2, SnO,Sn(OH)2, Al2O3, Al(OH)3, Fe2O3,Fe(OH)3, Cr2O3, Cr(OH)3
Свойства амфотерных соединенийзапомнить не сложно: они взаимодействуют с
Основания и амфотерные гидроксиды
«,»author»:»»,»date_published»:null,»lead_image_url»:»https://lh4.googleusercontent.com/proxy/yC-Ifc-0BLH4UA23up92hqFuYxQojD_vAH87Z7nrY13SsuAATwUNo3DZ5F_Evhhyax6bXZPv4ghyVZM92EOBb7XoSBI=w1200-h630-n-k-no-nu»,»dek»:null,»next_page_url»:null,»url»:»http://himija8en.blogspot.com/p/blog-page_23.html»,»domain»:»himija8en.blogspot.com»,»excerpt»:»ÐмÑоÑеÑноÑÑÑ (Ð¾Ñ Ð´Ñ.-гÑеÑ. амÑоÑеÑо â «двойÑÑвеннÑй», «обоÑднÑй») â ÑпоÑобноÑÑÑ Ð½ÐµÐºÐ¾ÑоÑÑÑ Ñоединений пÑоÑвлÑÑÑ Ð² завиÑимоÑÑи Ð¾Ñ …»,»word_count»:714,»direction»:»ltr»,»total_pages»:1,»rendered_pages»:1}