Меднение алюминия в домашних условиях
Меднение алюминия в домашних условиях — Станки, сварка, металлообработка
Гальваника – это и раздел прикладной науки «Электрохимия», в котором изучаются процессы, протекающие при осаждении катионов металла на катоде, помещенном в электролитический раствор, и технологический процесс. Гальваника в домашних условиях или выполняемая на производстве позволяет наносить на поверхность обрабатываемого изделия тонкий слой металла, который может выступать в роли защитного или декоративного покрытия.
Домашняя гальваническая установка
Методы реализации такого технологического процесса, отличающегося достаточно высокой сложностью, уже хорошо отработаны, поэтому сегодня его активно используют не только производственные предприятия, но и многие домашние мастера.
Особенности процесса
Покрытие, формируемое на обрабатываемой детали при помощи гальваники, может наноситься в технологических целях либо выполнять декоративные, защитные или сразу обе функции. В декоративных целях создают тонкий слой золота или серебра, а чтобы обеспечить надежную защиту поверхности обрабатываемой детали от коррозии, выполняют цинкование или гальваническое меднение.
Схема процесса электролиза
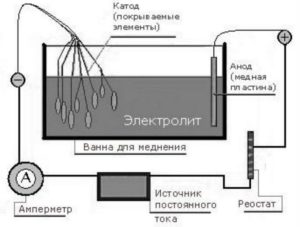
Сделать гальванику даже в домашних условиях несложно. Выполняют такую процедуру следующим образом.
- В диэлектрическую емкость с электролитом опускают два анода, подключаемые к плюсовому контакту источника электрического тока. Материалом изготовления таких анодов должен быть металл, слой из которого необходимо сформировать.
- Само обрабатываемое изделие, подключаемое к минусовому контакту источника электрического тока и, таким образом, выступающее в роли катода, помещается в электролите между анодами.
- Гальванизация, то есть процесс переноса молекул металла с электролита на изделие-катод, начинает происходить в тот момент, когда замыкается полученная электрическая сеть.
В результате на обрабатываемой поверхности формируется тонкий и однородный слой металла, который изначально содержался в химическом составе электролита.
Схема гальванической установки
Необходимое оборудование
Гальваника своими руками может быть качественно выполнена с использованием даже самого простейшего оборудования, которое есть в арсенале многих мастеров.
В первую очередь следует подобрать источник постоянного тока, который обязательно должен быть оснащен регулятором выходного напряжения.
Наличие такого регулятора необходимо для того, чтобы иметь возможность плавно и в широких пределах изменять мощность вашего самодельного устройства для гальваники.
В качестве источника питания в домашних условиях очень удобно использовать выпрямитель электрического тока, который можно собрать самостоятельно (или приобрести серийную модель). Многие умельцы, выполняющие нанесение гальванического покрытия в домашних условиях, в качестве источника тока применяют серийные сварочные аппараты.
Для домашней гальваники подойдет стабилизированный блок питания с регулируемым напряжением (1,5–12 В)
Гальваническая ванна своими руками также может быть изготовлена без особых проблем.В качестве такой ванны можно использовать любую емкость из стекла или пластика, при этом необходимо учитывать, что в такую емкость для гальваники должна помещаться как обрабатываемая деталь, так и требуемое количество электролита. Очень важно также, чтобы ванна была достаточно прочной и могла выдерживать высокую температуру, величина которой может доходить до 80°.
Аноды, используемые для осуществления гальваники в домашних условиях, выполняют сразу несколько важных функций:
- подводят в электролит электрический ток и обеспечивают равномерное распределение последнего по обрабатываемой поверхности;
- возмещают убыль наносимого на изделие металла, расходуемого из химического состава электролита;
- способствуют протеканию некоторых окислительных процессов.
Выбирая аноды для своего гальванического аппарата, следует соблюдать одно важное правило: их площадь должна быть больше, чем площадь обрабатываемой поверхности.
Гальваника дома не может быть осуществлена без использования нагревательного прибора, при помощи которого электролит доводится до требуемой рабочей температуры. Очень удобно, когда интенсивность нагрева, обеспечиваемого таким устройством, может регулироваться.
Если ориентироваться на опыт домашних умельцев, которые уже имеют опыт нанесения гальванических покрытий в домашних условиях, можно порекомендовать использовать в качестве нагревательного прибора небольшую электроплитку или обычный утюг с регулировкой степени нагрева подошвы.
Что потребуется для приготовления электролита
Чтобы безопасно хранить в домашних условиях химические реактивы, из которых будет готовиться электролит для гальваники, а также сам готовый раствор, вам потребуется стеклянная посуда с притертыми крышками.
Количество химических реактивов, из которых готовится электролитический раствор, необходимо отмерять с точностью до одного грамма.
Для решения такой задачи в домашних условиях подойдут даже недорогие электронные весы, которые можно приобрести в любом хозяйственном магазине.
Готовый электролит можно слить и в пластиковую бутылку, но для кислотных составов нужно использовать стеклянную посуду
Если вы решили заняться нанесением гальванических покрытий на различные изделия в домашних условиях, то наверняка столкнетесь с проблемой приобретения химических реактивов, из которых готовится электролитический раствор.
Дело в том, что организации, производящие и реализующие такие химические вещества, могут продавать их только тем, кто имеет соответствующие разрешительные документы.
Приобрести такие химические реактивы частному лицу или даже организации, не обладающим такими документами, проблематично.Для нанесения декоративных металлизированных покрытий можно приобрести специальные комплекты, состоящие из всех необходимых компонентов
Как правильно подготовить изделие к процедуре
После того как вы изготовили свой гальванический аппарат, нашли все необходимое оснащение и химические составляющие, можно приступать к такому важному процессу, как подготовка изделия, которое будет подвергаться гальванике. Важность такого процесса очень сложно переоценить, так как именно от качества его выполнения во многом зависит то, какими характеристиками будет обладать готовое покрытие.
В большинстве случаев подготовка изделия к гальванике не ограничивается только очисткой его поверхности от загрязнений и ее обезжириванием. Выполняются также пескоструйная обработка и последующая шлифовка с использованием наждачной бумаги и специальных паст.
Гальваническое покрытие выделяет все недостатки поверхности, поэтому обрабатываемая деталь должна быть идеально подготовлена, то есть устранены все сколы, царапины и раковины
Для того чтобы обезжирить обрабатываемую поверхность перед гальваникой, можно использовать органические растворители в чистом виде или приготовить для этих целей специальный раствор.
В частности, для эффективного обезжиривания стали или чугуна в домашних условиях готовят растворы, в состав которых входят едкий натр, жидкое стекло, карбонат натрия и фосфат натрия. Обезжиривание изделий из таких металлов выполняют в нагретом до 90° растворе.
Цветные металлы можно эффективно обезжирить растворами, содержащими в своем составе хозяйственное мыло и фосфорнокислый натрий.
Составы щелочных обезжиривающих растворов
Чтобы получить качественное гальваническое покрытие как в домашних, так и в производственных условиях, с обрабатываемой поверхности необходимо также удалить окисную пленку, для чего используют специальные декапирующие растворы с серной или хлороводородной кислотой.
Требования техники безопасности
Любая гальваническая операция (цинкование, хромирование, никелирование, меднение и др.
) является опасным технологическим процессом, поэтому при ее выполнении в домашних условиях необходимо строго следовать требованиям техники безопасности.
Опасной гальванику делают как токсичные химические вещества, так и высокая температура нагрева электролита, а также риски, связанные с любыми электрохимическими процессами.
Для проведения гальваники в домашних условиях лучше отвести нежилое помещение, в качестве которого может выступать гараж или мастерская. В нем обязательно должна быть организована качественная вентиляция. Все электрическое оборудование, которое вы будете использовать для того, чтобы сделать гальванику, необходимо заземлить.
Резиновые перчатки, очки и респиратор – минимум необходимых защитных средств
Личная безопасность – самое важное правило, которого следует строго придерживаться при осуществлении гальваники в домашних условиях. К мерам, которые способны обеспечить такую безопасность, следует отнести:
- использование респиратора для защиты дыхательных путей;
- защита рук при помощи мягких и прочных резиновых перчаток;
- использование при работе клеенчатого фартука и обуви, способной защитить от ожогов кожу ног;
- защита органов зрения при помощи специальных очков.
Меднение алюминия в домашних условиях — Металлы, оборудование, инструкции
Процесс меднения металлических изделий называется гальваностегией. Он основан на осаждении на поверхность деталей другого металла, растворимого в специальной жидкости.
Технология омеднения включает изготовление раствора и создание разноименных электродов. В процессе гальваностегии, ионы меди, растворенные в электролите, притягиваются отрицательным полюсом (обрабатываемая деталь) на свою поверхность.
Омеднение различных деталей в промышленных масштабах применяется не только, как конечный процесс обработки поверхности металлических изделий. Он может использоваться для подготовки деталей к следующей операции, например, никелированию, серебрению или хромированию изделий.
Эти металлы плохо осаждаются на поверхность стальных деталей, а на омедненную поверхность ложатся очень хорошо. В свою очередь медь, осевшая на стальные детали, держится прочно и способствует выравниванию различных дефектов на ее поверхности.
Меднение деталей в растворе с электролитом
Для металлических деталей можно выполнить меднение в домашних условиях. Рассмотрим меднение, с опусканием детали в раствор с электролитом. Для этого необходимо иметь:
- небольшие медные пластины,
- несколько метров токопроводящей проволоки;
- источник тока, с напряжением до 6 В;
- рекомендуется также использовать реостат, для регулирования тока и амперметр.
Порядок работы
- В качестве жидкости, хорошо растворяющей медь, применяется обычный электролит. Его можно купить или приготовить в домашних условиях. Для этого потребуется 3 мл серной кислоты, на каждые 100 мл дистиллированной воды. Необходимый раствор, можно получить, добавив в полученный электролит до 20 гр. медного купороса.
- Перед началом процесса меднения детали, ее необходимо очистить наждачкой, чтобы снять оксидную пленку с поверхности.
- Затем, деталь обезжиривается горячим содовым раствором, и промывается чистой водой.
- В стеклянную емкость, нужного объема, наливается приготовленный раствор электролита.
- Затем, туда опускаются две медные пластины, на токопроводящих проводах. Между двумя медными пластинами подвешивается, предназначенная для меднения в домашних условиях деталь, на аналогичном проводе. Необходимо проследить, чтобы медные пластины и деталь были полностью залиты раствором электролита.
- На следующем этапе, концы проводов от медных пластин подсоединяются к плюсовой, а обрабатываемая деталь к минусовой клеммам источника тока. Последовательно, в созданную электрическую цепь нужно подсоединить реостат и амперметр. После включения тока в цепи, он реостатом устанавливается в пределах 15 мА на 1 см? площади поверхности детали.
- Выдержав, обрабатываемую деталь в растворе, в пределах 15-20 минут, нужно выключить электропитание и извлечь изделие из раствора. За этот непродолжительный промежуток времени, поверхность детали покроется тонким слоем меди. Толщина покрытия будет зависеть от продолжительности процесса меднения. Таким образом, можно достичь меднения поверхности любого изделия слоем в 300 мкм и более.
Меднение детали, без опускания в раствор
Второй способ меднения в домашних условиях металлических изделий, подразумевает выполнение этого процесса без опускания обрабатываемой детали в раствор электролита.
Этот вариант подходит для нанесения покрытия на цинковые и алюминиевые изделия.
Порядок работы
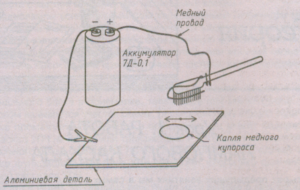
- Для этого способа меднения потребуется многожильный медный провод, с двух концов которого, необходимо снять изоляцию. С одной стороны мягкий провод нужно растеребить. Таким образом получается изделие в виде кисточки. Чтобы удобнее в дальнейшем было работать, к этому концу провода нужно привязать твердый предмет в виде рукоятки. Второй очищенный конец провода нужно соединить к положительной клемме источника электрического тока. Напряжение не должно превышать 6 В.
- Ранее описанным способом нужно приготовить электролит, размешанный с медным купоросом. В этом методе меднения деталей, раствор можно наливать в любую посуду. Рекомендуется выбрать широкую тару, чтобы было удобно макать медную кисточку из проволоки. Далее необходимо небольшую металлическую деталь положить в эту посуду, с невысокими краями. Предварительно ее нужно очистить, прокипятить в жидкости со стиральным порошком, и промыть. Эту деталь нужно соединить с помощью провода к отрицательной клемме источника тока, с напряжением 6 В.
- Процесс меднения происходит следующим образом. Растеребленный конец медной проволоки нужно периодически обмакивать в растворе электролита, с медным купоросом и проводить вдоль детали, не прикасаясь «кистью» к ее поверхности. Но нужно предусмотреть, чтобы между концом кисти и деталью был небольшой слой раствора (катод и анод должны быть всегда смочены электролитом). В процессе меднения отрицательно заряженная деталь притягивает ионы меди и ее поверхность покрывается небольшим красным слоем. После нанесения покрытия, изделие нужно высушить и натереть до блеска.
Таким меднением, без погружения изделия в электролит, чаще обрабатываются детали больших размеров. Они не вмещаются в подобранную посуду с электролитом, и поверхность обрабатывается кистью небольшими участками.
руководство по меднению деталей в домашних условиях
Секреты меднения в домашних условиях
На самом деле, меднение в домашних условиях проводят многие умельцы в первую очередь для того, чтобы подготовить поверхность металла к последующей обработке различными защитными слоями.
Данной операции можно подвергать поверхности самых разных металлов и неметаллов, в том числе, стали, латуни, никеля и так далее.
Человечество используется в своих целях медь на протяжении многих тысячелетий и связано это, прежде всего с тем, что данный металл находится в природе в самородном состоянии, а кроме этого, обладает рядом уникальных свойств.
В настоящее время медь и самые разные сплавы на ее основе востребованы во многих промышленных сферах.Без нее не может обойтись авиастроение, автомобилестроение, приборостроение и многие другие отрасли.
Медь и ее многочисленные сплавы достаточно распространены и в бытовой сфере.
Следует отметить и то, что добавки меди в различных сочетаниях позволяют эффективно защитить поверхности многих металлов, например, стали, латуни или никеля от различных агрессивных сред.
Один из наиболее распространенных способов покрыть тонким слоем металлическую поверхность — это выполнить нанесение меди.
В условиях дома в большинстве случае выполняется химическое меднение, причем существует несколько различных способов, каждый из которых имеет как свои плюсы, так и минусы.
Один из способов выполнить гальваническое нанесение меди в условиях дома, показан на видео ниже.
:
- Характеристики металла
- Особенности меднения
- Способы нанесения
Характеристики металла
Как уже было сказано выше, в природе медь, как правило, находится в виде небольших самородков.
Это уникальное вещество представляет собой достаточно тяжелый металл, который на вид напоминает самородок яркого розово-красного оттенка.
Этот металл обладает относительной мягкостью и высокой ковкостью, кроме этого, имеет температуру плавления порядка тысячи ста градусов по Цельсию.
Он великолепно проводит не только тепло, но и электрический ток, что и объясняет повышенный спрос на данный металл в электротехнике и приборостроении.
В большинстве случаев в природе медь находится не в чистом состоянии, а с различными примесями.
Всевозможные природные добавки в зависимости от различных факторов в металле могут варьироваться и различаться приблизительно от десяти до пятидесяти раз.
Для данного металла большое значение имеет содержание в нем кислорода, и в зависимости от количества этого элемента в состав меди, разработана определенная классификация.Так, медь может быть бескислородной и рафинированной.
Помимо данного элемента в этом металле также может находиться водород, попадающий туда за счет электролиза или отжига.
Медь имеет определенную кристаллическую решетку, и атомы водорода занимают в ней пространство в междоузлиях, а это значит, что на ее свойства они не оказывают практически никакого влияния.
:
Если медь в своем составе содержит в определенном количестве кислород, то водород имеет свойство определенным образом взаимодействовать, но только при достаточно высоких температурах с медной закисью, и в этом конкретном случае начинает формироваться водяной пар, который имеет достаточно высокие показатели давления.
Это оказывает негативное влияние на металл в целом и может привести в некоторых случаях к образованию вздутий, а также трещинам и разрывам.
Такое отрицательное воздействие у химиков получило название водородная болезнь.
На изменении показателей пластичности у меди в худшую сторону могут оказать влияние присутствие железа, сурьмы.
Те примеси, которые относятся к группе малорастворимых, понижают хрупкость этого металла, но только при достаточно высоких внешних температурах, а это значит, что для меди крайне нежелателен процесс обработки горячим давлением.
На видео выше показано химическое меднение данного металла.
Особенности меднения
Для выполнения меднения на поверхности стали, никеля, либо каких-то других металлов, применяется гальваника, при которой образуется тонкий медный слой.
Гальваническое нанесение меди представляет собой достаточно сложное химическое меднение, которое оказывает влияние на состав материала.
Гальваническое нанесение является предварительным, перед тем, как на поверхность никеля или другого металла будет нанесен различный защитный состав.
Химическое и гальваническое меднение: состав и подготовка

Современная техника выдвигает жесткие требования к характеристикам конструктивных элементов, во многих случаях эти задачи решает химическое меднение. Использование специальных покрытий поверхностей деталей выгодно экономически, так как гальваническое меднение позволяет понизить металлоемкость изделий из дорогостоящих металлов.
Физико-механические характеристики меди и сферы использования меднения
Плотность меди 8,96 г/см3, атомная масса 693,54, удельное электрическое сопротивление 1,68×10-8 Ом×м, температура плавления +1083°С.
На открытом воздухе в присутствии агрессивных химических соединении медь окисляется, при контакте с сернистыми соединениями покрывается пленкой сульфида меди темно-коричневого или серого оттенков.
Под влиянием углекислоты и влаги пленка приобретает зеленый цвет, верхний слой состоит из гидрокарбонатов. Медь легко растворяется в растворе азотной кислоты, разбавленная серная кислота на химическое меднение негативного влияния почти не оказывает.Но наличие кислорода увеличивает скорость протекания химических реакций. При наличии открытых пор в покрытии образуется гальванопара, что нужно учитывать при меднении. Железо в этом случае является анодом, коррозионные процессы протекают очень интенсивно.
В связи с такими особенностями, процесс меднения в большинстве случаев должен завершаться дополнительной обработкой поверхностей. Покрытия шлифуются или полируются до зеркального блеска. Медь имеет высокую адгезию с различными металлами: алюминий, серебро, цинк, никель, свинец, хром и т. д.
В связи с этими особенностями химическое меднение часто используется для создания подслоя при серебрении, никелировании, хромировании поверхностей деталей. Меднение получило широкое распространение в качестве метода эффективной защиты отдельных участков деталей от появления эффекта науглероживании при процессе цементации.
В зависимости от назначения деталей или изделий гальваническое нанесение меди может иметь следующую толщину:
Толщина слоя меди на поверхности обрабатываемых деталей
Сравнительные показатели растворов
В процессе меднения используется большое количество специальных технологических растворов, разделяемых на две большие группы:
- Простой кислый электролит. Из простых применяется фторборатный, кремнефторидный, сульфатный, хлоридный и сульфамидный раствор.
- Комплексный электролит. Преимущественно щелочные, медь присутствует как положительно или отрицательно заряженные комплексные ионы.
График поляризационных кривых осаждения меди из различных типов электролитов
Процесс осаждения в кислых электролитах происходит при высокой плотности по току, они устойчивы, просты по химическому составу.
Главными составляющими являются соответствующие кислоты и соли, осадки меди из них достаточно плотны и имеют крупнокристаллическую структуру.
Недостатки – непосредственное меднение стали, цинковых сплавов и иных металлов происходит с более низким отрицательным потенциалом, чем медь.
Обработка деталей в комплексных электролитах выполняется за счет комплексных ионов, для них требуется высокая катодная поляризация. Выход по току меньше, что способствует более равномерному осаждению, структура мелкокристаллическая. Используются пирофосфатные, цианидные, аммонийные, триполифосфатные, цитратные и другие растворы.
Способность рассеивания электролитов для меднения
Простые кислые составы
- Сульфатные. Главные компоненты серная кислота и сульфат меди. Сернокислое соединение отличается невысокой электропроводимостью, для повышения параметра добавляется серная кислота. Выход меди по току достигает 100%, на катоде не выделяется водород. За счет повышения концентрации кислоты уменьшается растворимость сульфата, что понижает верхний предел максимально допустимой плотности тока.
Влияние содержания серной кислоты на электропроводность электролита
При перемешивании увеличивается концентрация медных ионов на катодном слое. При повышении температуры возрастает растворимость сульфата меди, электролит повышает кислотность, что приводит к получению мелкокристаллических осадков.
Для улучшения катодной поляризации в электролит добавляются поверхностно активные вещества. Дополнительно они уменьшают образование наростов на острых краях.
Режимы и состав сульфатных электролитов для меднения
Для образования блестящего покрытия используются аноды АМФ, не допускающие образование шлама, или аноды из особо чистой рафинированной меди.
Влияние концентрации меди на плотность тока с перемешиванием (1) и без перемешивания (2). Электролит фторборатный.Электролит фторборатный.
Для недопущения попадания шлама аноды помещаются в чехлы, изготовленные из кислотоустойчивого материала, дополнительно раствор постоянно фильтруется.
- Фторборатные. Отличаются высокой устойчивостью, гальваническое нанесение получается плотным и мелкокристаллическим, рассеивающие показатели такие же, как при сульфатном меднении. За счет большой растворимости увеличивается плотность тока, осаждать медь непосредственно на детали нельзя.
Состав и режим работы фторборатных электролитов
При непрерывном перемешивании допускается повышать плотность тока. Контроль технологически параметров меднения осуществляется измерением кислотности раствора. Для повышения качества меднения используется карбонат натрия, для понижения медный купорос.
- Нитратные. Электролит используется при гальванопластике, обеспечивает повышенное качество осадка.
Режимы и состав нитратных электролитов
Комплексные электролиты
- Цианидные. Условия обработки значительно отличаются от осаждения из кислых, в них медь существует в виде комплексных ионов, что заметно понижает ее активность. Увеличение плотности тока принуждает катодный потенциал резко смещаться в поле отрицательных значений. Но процесс меднения нельзя производить при увеличенной плотности тока в связи с тем, что выход меди может падать до нуля. Главными компонентами раствора являются свободный цианид натрия и комплексный цианид калия. Во время работы содержание меди понижается из-за недостаточной их растворимости.
Режим и состав цианидных электролитов для меднения
- Пирофосфатные. Медные осадки имеют мелкокристаллическую структуру, гладкие, блестящие или полублестящие. Для улучшения качества обработки и повышения катодной и анодной плотностей может добавляться медный купорос. Катодный потенциал в пирофосфатных растворах имеет более отрицательные параметры, чем у кислотных.
Режим и состав пирофосфатных электролитов
- Этилендиаминовые. Процесс меднения может осуществляться непосредственно по поверхности стали, при низких плотностях тока катодная поляризация достигает больших значений. Рассеивающие характеристики выше, чем у сульфатных, но ниже, чем имеет цианидный раствор.
Режим и состав этилендиаминовых электролитов
Загрузка и выгрузка деталей должна выполняться при минимальной силе тока, в первые 40–50 секунд дается толчок тока, в три раза превышающий рабочие значения меднения.
- Полиэтиленполиаминовые. Во время обработки деталей потенциалы смещаются в поле отрицательных значений, электролит применяется вместо цианидных.
Режим работы и составы полиэтиленполиаминовых электролитов
- Аммонийные. В состав входит аммиак, сульфат аммония и сульфат меди. При невысоких плотностях тока уменьшается выход по току, улучшение меднения осуществляется за счет добавления нитрата аммония. Осадки равномерные по толщине, плотные и полублестящие.
Режимы работы и состав аммонийного электролита
Без специальной обработки поверхностей медные осадки имеют недостаточную адгезию, причина – пассивирование стали раствором аммиака. Улучшение параметров покрытия достигается введением в раствор нитрата меди.
Устройство ванны медненияЛинейные параметры и конструктивные особенности должны отвечать требованиям ГОСТ 23738-85.
Гальваническая ванна изготавливается из модифицированных особо устойчивых пластиков, конкретные марки подбираются с учетом параметров технологических процессов.
Ванна без кармана. Наиболее простая конструкция, применяется как в отдельности, так и на производственных линиях.
Ванна без кармана
Ванна с карманом. Обработка может выполняться с одновременными процессами удаления верхнего загрязненного слоя электролита.
Ванна с карманом
Конкретный выбор ванны меднения осуществляется в зависимости от особенностей предприятия, характеристик подлежащих меднению деталей и общих производственных мощностей.
Во время проектирования рассчитываются максимальные нагрузки с учетом объема раствора, длина, высота и ширина может изменяться по желанию заказчиков.
При необходимости на ванны меднения устанавливается дополнительное оборудование и водопроводная арматура. За счет специальных механизмов улучшается качество процесса меднения.Используемые пластики адаптируются к химическому составу электролита и температурным режимам меднения.
Механическая подготовка поверхностей
Перед меднением с поверхности должна удаляться окалина, заусеницы и раковины. Качество обработки регламентируется положениями действующего ГОСТа 9.301-86. Конкретные параметры шероховатости устанавливаются в зависимости от назначения покрытия.
После механической обработки деталей с поверхности должны быть удалены все дефекты, оказывающие негативное влияние на качество меднения.
В обязательном порядке удаляется техническая смазка и эмульсия, металлическая стружка, продукты коррозионных процессов и пыль.
Подготовка к меднению производится при следующих технологических операциях:
- Шлифование. Верхний слой деталей снимается абразивными элементами, может быть тонким, декоративным или грубым.
- Полирование. Во время операции сглаживаются мельчайшие выступы, поверхность блестящая зеркальная.
- Крацевание. Для очистки поверхностей применяются металлические щетки.
- Галтовка. Детали обкатываются в специальных колоколах.
- Химическое и электрохимическое обезжиривание. Для обработки используют органические и неорганические растворы.
От качества предварительной подготовки поверхностей во многом зависит процесс меднения и физические показатели осадков.
Покрытие алюминия медью в домашних условиях

Как медь сделать золотом, сталь медью, а алюминий серебром? Речь пойдёт об окрашивании металлов в различные цвета и оттенки других металлов.
Существуют различные способы придания окрасок металлам: химические, электрохимические, применение различных паст. Все способы рассмотрим ниже.
Способы серебрения металлов
Простой способ серебрения
В качестве серебрящего состава применяют обработанный гипосульфит (фотофиксаж), уже непригодный для закрепления плёнок и фотобумаги.
Медную деталь зачищают до блеска, кипятят в содовом растворе и тщательно промывают водой. Затем опускают в использованный гипосульфит. Через некоторое время на деталь осядет серебро.
После промывки водой деталь сушат и полируют суконкой. Качество серебрения и прочность сцепления серебра с медью зависит от концентрации серебра в растворе гипосульфита.
Серебрение металлических деталей горячим способом
Этим способом можно серебрить любые металлы. Заключается он в следующем. Чисто обработанную деталь погружают на цинковом центе в кипящий раствор:
- железосинеродистый калий — 120 г.;
- поташ — 80 г.;
- хлористое серебро — 7,5 г.;
- дистиллированная вода до 1 литра.
Процесс серебрения оканчивается после полного покрытия серебром поверхности детали. Затем деталь вынимают из раствора, промывают и полируют.
Внимание! Следует помнить, что при кипении раствора выделяются вредные вещества, поэтому кипячение следует производить на открытом воздухе или под вытяжкой.
Химическое серебрение
1) Несколько листов матовой фотобумаги (не для принтера, а бумага для проявления фото с плёнки), разрезают на куски и опускают в раствор фиксажной соли (соль разводят в том объёме воды, как сказано на упаковке).
Зачищенную и обезжиренную деталь помешают в этот раствор и натирают эмульсионным слоем бумаги до тех пор, пока на поверхности детали не образуется плотный слой серебра.
После промывки в тёплой воде деталь протирают сухой ветошью.
2) В 300 мл. отработанного фиксажа (например, оставшегося после печатания фотографий) добавляют 1-2 мл. нашатырного спирта и 2-3 капли формалина (раствор хранят и работают с ним только в темноте). Зачищенную и обезжиренную деталь помещают в раствор на пол часа (до полутра часов), затем промывают в тёплой воде, высушивают и протирают мягкой ветошью.
Приготовление и применение пастообразной смеси для серебрения
Детали из меди, латуни, медного железа, можно посеребрить с помощью паст.
1. В 300 мл. дистиллированной воды или простой воды, полученной из льда бытовых холодильников, растворяют 2 г. азотнокислого серебра (ляписа) и к раствору подливают 10% раствор поваренной соли до тех пор, пока не прекратиться выпадение осадка хлористого серебра. Этот осадок 5-6 раз промывают в проточной воде.
Отдельно в 100 мл дистиллированной воды растворяют 20 г. гипосульфита и 2 г. хлористого аммония (нашатыря). Затем в раствор небольшими дозами добавляют хлористое серебро до тех пор, пока оно не прекратит растворяться. Полученный раствор фильтруют и смешивают с мелко размолотым мелом до консистенции густой сметаны.
Заранее обезжиренную деталь натирают пастой с помощью ваты или марли до образования на её поверхности плотного слоя серебра, после чего деталь промывают водой и протирают сухой ветошью.
2. Отполированную и обезжиренную деталь протирают тканью или куском мягкой кожи, на которую нанесена паста такого состава:
- хлористое серебро — 6 г.;
- поваренная соль — 8 г.;
- кислый виннокислый калий (винный камень) — 8 г.
Перечисленные вещества растирают в ступе и хранят в темной посуде, перед применением смесь разводят дистиллированной водой до получения жидкой пасты.
Когда деталь покроется слоем серебра, её промывают в воде и натирают до блеска мягкой фланелью.
3. Пасту для серебрения приготавливают так: в сосуд насыпают 2г. нашатыря, 4г. винного камня и 2г. азотнокислого серебра, добавляют немного дистиллированной воды до получения жидкой кашицы. Затем тканью с нанесенной на неё пастой отполированную и обезжиренную деталь натирают до серебряного блеска.
Окраска меди под золото
В 100 г. воды растворяют 4 г. каустической соды и 4 г. молочного сахара, кипятят 15 минут, затем при постоянном размешивании прибавляют малыми дозами 4 г. раствора насыщенного медного купороса. В горячую смесь погружают хорошо очищенные медные изделия.
https://www..com/watch?v=lIL4ikGCdP4
В зависимости от продолжительности действия они приобретают различную окраску — от золотой, зелёной до полной черноты.
Химическое покрытие металлов
Деталь, подлежащую декоративному никелированию, необходимо подготовить: отшлифовать, при необходимости, отполировать и обязательно обезжирить.
Стальные детали обезжиривают в растворе, содержащим на 1 литр воды 20-30 грамм едкого калия (или едкого натра), 25-50 г. кальцинированной соды и 5-10 г. жидкого стекла (силикатного клея); медные — в растворе, содержащем (на то же количество воды) 100г. тринатрифосфата и 10-20 г. жидкого стекла.
Перед никелированием медные детали необходимо подержать на железе 30-60 сек. Следует также иметь ввиду, что сплавы, содержащие более 1-2% свинца или кадмия, химическому никелированию не поддаются.
Обезжиривание стальных и медных деталей при комнатной температуре заканчивается через 40-60 минут, при температуре 75-85 °С — через 20-30 минут.Затем деталь тщательно промывают в проточной воде и погружают на минуту в 5% раствор соляной кислоты для снятия плёнки окислов, после чего ещё раз промывают в воде и сразу переносят в раствор для никелирования. В 1 литре воды нагретой до 60 °С растворяют 30 г.
хлористого никеля и 10 г. уксуснокислого натрия. Затем температуру раствора доводят до 80 °С, добавляют 15 г. гипофосфата натрия — и раствор готов.
В него погружают деталь, доводят температуру до 90-92 °С и поддерживают её на этом уровне до окончания процесса никелирования. При понижении температуры скорость процесса резко замедляется, а при нагревании выше 95 °С раствор может испариться.
Необходимое количество раствора зависит от площади детали. Отношение этой площади в квадратных дециметрах (дм2) к объёму раствора (в литрах) должно быть в пределах 2,5-3,5. Так, например, при отношении объёма к площади равным 3 за 1 час толщина слоя никеля составит 10 микрон (мк).
Применяемые химикаты не ядовиты, обезжиривание и никелирование не сопровождается выделением вредных газов.
Химическое меднение стальных и чугунных деталей.
Состав электролита:
- сернокислая медь — от 8 до 50 г.;
- серная кислота концентрированная — 8-50 г.;
- вода до 1 л.
Рабочая температура 18-20 °С. После тщательной очистки и обезжиривания детали погружают на несколько секунд в раствор. Детали, покрытые медью, извлекают из раствора, промывают водой и сушат.
Химическое хромирование металлов.
Детали из стали меди и латуни химически хромируют в следующем растворе:
- фтористый хром — 14 г.;
- гипосульфат натрия — 7г.;
- лимоновокислый натрий — 7г.;
- уксусная кислота ледяная — 10мл.;
- едкий натрий (20%) — 10 мл.;
- вода до 1л.
Рабочая температура 80 °С. Очищенные и обезжиренные детали металлизируют в течение 6-8 часов. При химическом хромировании стальных предметов рекомендуется сначала их химически «помеднить». Детали с осаждённым слоем хрома промывают в воде и сушат.
Химическое никелирование металлов производят в следующем растворе:
- сернокислый никель аммоний — 50г.;
- хлористый аммоний — 40 г.;
- вода до 1 л.
В раствор добавляют небольшое количество металлического цинка и непрерывно его перемешивают.
Химический способ лужения металлов.
Детали из стали, меди, латуни химически лужат в растворе:
- хлористое олово — 10 г.;
- молочнокислый натрий — 100 г.;
- вода до 500мл.
Весь процесс проводится при температуре раствора 18-20 °С. Перед лужением детали так же очищают и обезжиривают.
Для мелких деталей применяется следующий паствор:
- хлористое олово — 5 г.;
- сернокислый алюминий-аммоний (алюмо-амонные квасцы) — 150 г.;
- вода до 500 мл.
Изделия и детали из силулина (сплав алюминия с кремнием) быстро покрывается окисной пленкой темных тонов. Однако они длительное время могут быть блестящими, если их осветлить.
Изделия или детали зачищают и, если надо, полируют и погружают на 10-20 минут в следующий раствор:
- хромовый ангидрид — 100 г.;
- серная кислота концентрированная — 10 г.;
- вода до 1 литра.
Рабочая температура в пределах 18-20 °С. После осветления изделия и детали промывают и сушат, а чтобы поверхности изделий и деталей не окислялись длительное время их покрывают бесцветным лаком.
Окрашивание электрохимическое
Для электрохимического окрашивания деталей из стали, латуни или меди необходимо собрать гальваническую ванну и электросхему (с резистором в 150 Ом на плюс). Электрод подключаемый к плюсу делают из листовой меди, отрицательный контакт подключают к окрашиваемой детали через специальный зажим.
Необходимо следить, чтобы деталь не касалась медной пластинки.
В банку заливают специальный электролит и замыкают цепь. Через 2-3 минуты начинается окрашивание. Вначале деталь станет коричневой, потом фиолетовой и т.д.
Всё будет зависеть от времени:
- 2 минуты — коричневый цвет;
- 3 мин. — фиолетовый;
- до 5 мин. — синий;
- 5-6 мин. — голубой;
- 8-12 мин. — жёлтый;
- 12-13 мин. — оранжевый;
- 13-15 мин. — красный;
- 17-21 мин. — зелёный цвет.
Состав раствора электролита:
- медный купорос — 60 г.;
- сахар рафинад — 90 г.;
- едкий натр — 45 г.
Приготовляют электролит следующим образом. В раствор медного купороса =200-300 мл. добавляют сахар и тщательно размешивают. Отдельно в 250 мл. воды растворяют едкий натр, и к нему небольшими порциями, постоянно помешивая, приливают раствор медного купороса с сахаром. Затем добавляют воду, чтобы получился 1 литр раствора.
Чтобы цвета окрашиваемых изделий были более контрастными, в готовый электролит добавляют 20 грамм безводной соли углекислого натрия. После окрашивания деталь промывают водой, сушат, покрывают бесцветным лаком.
Внимание! При работе с едким натром необходимо соблюдать осторожность!
Растворы электролитов для гальванических ванн
Электролит для быстрого меднения:
- сернокислая медь (медный купорос) — 250 г.;
- серная кислота концентрированная — 20 г.;
- хромовый ангидрид — 2 г.;
- вода — до 1 литра.
Рабочая температура 18-25 °С, рекомендуется перемешивание, плотность тока = 5А/дм2.
Электролит для матового никелирования:
- сернокислый никель — 217,5 г.
- хлористый никель — 46,5 г.
- борная кислота — 31 г.
- вода — до 1 литра.
Рабочая температура ванны 50-70 °С, плотность тока 1,5-5 А/дм2, кислотность среды (PH) 5,2-5,8.
Электролит для никелирования (твёрдое покрытие):
- сернокислый никель — 150 г.;
- хлористый аммоний — 20 г.;
- борная кислота — 25 г.;
- вода до 1 литра.