При какой температуре плавится металл
Температура плавления золота: чему равна, способы расплавить жёлтый металл в домашних условиях
Здравствуйте, мои читатели! В детстве я думал, что если прокипятить мамино кольцо в кастрюльке, оно расплавится.
Мне очень хотелось увидеть, как плавится металл, и я успел провести с десяток экспериментов, пока мама не узнала, что у нее растет металлург.
Ни один опыт не увенчался успехом, потому что температура плавления золота 1064,4 °C (градуса по Цельсию), а вода кипит всего при 100 °C.
Теперь я вырос и знаю, что все не так просто. Но плавление золота дома все же возможно, правда, для этого требуется нечто большее, чем просто кастрюлька и газ.
Характеристики и свойства металла
Золото — среднеплавкий металл: такими считаются те, что плавятся (переходят из твердого состояния в жидкое) при температуре от 600 °C до 1600 °C.
Под определение среднеплавких подходят многие металлы (никель, железо, кобальт, серебро) и сплавы (сталь, латунь, чугун). Золото можно плавить при помощи приспособлений, пригодных для большинства металлов.
Температура кипения золота — 2700 °C. Кроме того, оно обладает:
- высокой пластичностью и ковкостью;
- очень высокой плотностью;
- низкой твердостью.
Из слитка чистого золота можно выковать тонкую проволоку, не прибегая к использованию высокотехнологичного оборудования. Обладая несложным инструментарием и навыками, теоретически это возможно даже дома, потому что золото очень податливо и легко поддается обработке.
Как происходит переработка золотого сырья
Перед тем как превратиться в слиток, монету или украшение, драгметалл проходит многоэтапную обработку.
Шихта — материал, подлежащий отправке в плавильную печь — может состоять как из крупиц золота, добытого в природе, так и из лома (часового, ювелирного, технического, стоматологического).
Предварительные манипуляции направлены на то, чтобы сделать эту смесь максимально однородной перед плавлением. Для этого заводы по переработке подвергают сырье таким процедурам:
- Механическая очистка: дробление крупных кусков, измельчение и просеивание под струей воды или раствора с добавлением абразива, который дополнительно отмывает шихту от грязи.
- Химическая очистка от примесей — аффинаж. Вариатны: амальгамирование, растворение в царской водке или выщелачивание — цианированием или при помощи теокарбамидных растворов.
- Осаждение металла из полученных растворов.
В результате очистки в распоряжении рабочего завода (или частного ювелира) оказывается золото — в количестве намного меньшем, чем исходная шихта, зато практически чистое.
Можно приступать к плавке.
При какой температуре плавится
Говоря о температуре 1064,4 °C, я имел в виду чистое золото 999 пробы. Мы с вами можем встретить его только в виде банковских слитков (или если сами займемся аффинажем). В ювелирном деле, промышленности и медицине используется разбавленный — легированный металл.
В украшения лигатура вводится для прочности, в припои — для повышения текучести и достижения нужных параметров сплава для пайки изделий каждой пробы (цвета, плавкости). Вот сравнительная таблица температур, при которых плавятся пробы с разным процентным и качественным содержанием лигатуры:
| Цвет | Проба | Au (золото) | Ag (серебро) | Pd (палладий) | Cu (медь) | t (°C) |
| желтый | 375 | ~37.5 % | ~10 % | ~3.8 % | остальное | 926–949 |
| желтый | 585 | ~58.5 % | ~8 % | нет | остальное | 878–905 |
| зеленый | 585 | ~58.5 % | ~30 % | нет | остальное | 835–880 |
| красный | 585 | ~58.5 % | нет | нет | остальное | 907–922 |
| желтый | 750 | ~75 % | ~17 % | нет | остальное | 920–930 |
| розовый | 750 | ~75 % | ~12.5 % | нет | остальное | 900–920 |
| белый | 750 | ~75 % | ~5 % | ~20 % | нет | 1270–1280 |
Какие металлы используются в золотых сплавах, как они меняют температуру плавления
Необходимость изменить температуру плавления сплава особенно часто возникает при изготовлении припоев. Понижают температуру плавления золота более легкоплавкие добавки:
- цинк;
- олово;
- магний;
- алюминий;
- серебро (незначительно).
Повышают температуру плавления более тугоплавкие металлы и их сплавы — в ювелирном деле и промышленности это в основном платиновая группа:
Большинство интерметаллических сплавов хрупкие, поэтому для создания украшений они почти не применяются, а к промышленному использованию годны ограниченно.
Способы плавления и температура процесса
На заводах для плавления золота есть специальные плавильные печи, где без труда создается температура 1200 °C и выше. Дома невозможно установить такую.
Ювелиры пользуются портативными плавильными печками, например индукционными.
Некоторые любители плавят металлы в микроволновых печах, но в такой микроволновке больше будет нельзя готовить еду — учтите это перед тем, как выбрать свой метод.
«Классический» способ частных золотодобытчиков и ювелиров, не работающих с большими объемами сырья, — газовая или бензиновая горелка с инжектором и тигель — огнеупорная емкость, подходящая по размеру.
Можно ли расплавить золото в домашних условиях
Можно! Но нужно подготовиться.
Необходимое оборудование и материалы
Для самостоятельного изготовления отливок потребуются:
- тигель для плавления — керамический или графитовый, устойчивый к высоким температурам;
- горелка и топливо для нее;
- металлические щипцы;
- форма, в которую вы будете переливать расплавленное золото (изложница);
- бура (тетраборат натрия, его можно купить в аптеке) в качестве флюса для очистки расплава;
- деревянная или графитовая палочка для помешивания;
- доступ к чистой воде;
- вспомогательные емкости, салфетки, защитные аксессуары (перчатки, маска).
Подготовка шихты
Скорее всего, имеющееся в наличии сырье можно уместить в ладони, поэтому не будем имитировать заводской технологический процесс, а просто проверим лом на наличие ненужного мусора. Если у вас в руках аффинированный металл, то, вероятно, он уже измельчен и пригоден к плавлению — его достаточно промыть.
Если наша шихта — ювелирный лом, переплавить мы его сможем, но на выходе получится не чистый слиток, а сплав неизвестной пробы (как правило, мы не знаем, что и в каких пропорциях входит в состав украшений). Лом нужно тщательно измельчить перед плавлением.
Процесс плавки
Не забудьте надеть перчатки, темные очки и морально подготовиться к плавлению. Плавить золото нужно в чистом просушенном тигле, посыпав бурой и тигель, и шихту. Когда смесь буры и золота станет однородной, нужно посыпать расплав порошком вторично.
Подносите пламя горелки к золоту аккуратно, особенно если оно находится в тигле в виде мелких крупиц, чтобы не сдуть частицы металла. Не направляйте пламя на само золото: для начала аккуратно поводите огнем над ним. Нагревайте тигель постепенно и осторожно.
Работа занимает от 10 минут и более в зависимости от качества сырья. Через некоторое время дайте золоту слегка застыть и посмотрите на него. Если по мере затвердевания расплав мутнеет, значит, процесс не окончен и нужно использовать буру снова.Когда характерный желтый блеск перестанет исчезать при остывании, плавление можно считать завершенным.
Получение отливок
Расплавленное золото заливается в подготовленную форму. Лучше, если она будет изготовлена из того же материала, что и тигель. Через несколько минут, когда слиток немного остынет, вы сможете взять его щипцами и опустить в воду.
Как очистить отливки
После того как бура сослужит свою службу и очистит расплавленное золото от лишних соединений, придется избавить слиток от остатков самой буры. Для окончательной очистки потребуются:
- соляная кислота — 20 мл;
- азотная кислота — 10 мл;
- дистиллированная вода — 0,5 л;
- огнеупорная колба;
- электроплитка.
Отливку нужно прокипятить в растворе кислот в течение 5 минут и промыть чистой водой. Эту часть эксперимента лучше проводить на открытом воздухе, например на дачном участке: испарения кислот токсичны.
Заключение
Мама больше не запрещает мне кипятить золотые вещи, а я, возможно, однажды соберусь подарить ей кольцо, которое отолью сам. Оставайтесь со мной — нас ждет еще много интересного!
Таблица температур плавления металлов
instrument.guru > Металлообработка > Таблица температур плавления металлов
Каждый металл или сплав обладает уникальными свойствами, в число которых входит температура плавления. При этом объект переходит из одного состояния в другое, в конкретном случае становится из твёрдого жидким.
Чтобы его расплавить, необходимо подвести к нему тепло и нагревать до достижения нужной температуры. В момент, когда достигается нужная точка температуры данного сплава, он ещё может остаться в твёрдом состоянии.
При продолжении воздействия начинает плавиться.
- Как происходит процесс
- В зависимости от градуса, при котором плавятся металлы, они разделяются на:
- Таблица характеристик
- Среди наиболее часто применяемых в быту элементов показатели температуры плавления такие:
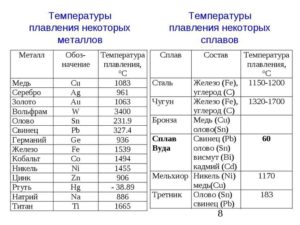
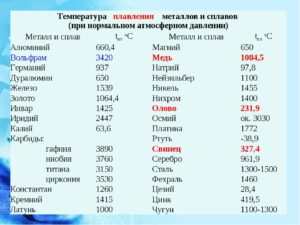
Наиболее низкая температура плавления у ртути — она плавится даже при -39 °C, самая высокая у вольфрама — 3422 °C. Для сплавов (стали и других) определить точную цифру крайне сложно. Все зависит от соотношения компонентов в них. У сплавов она записывается как числовой промежуток.
Как происходит процесс
Элементы, какими бы они ни были: золото, железо, чугун, сталь или любой другой — плавятся примерно одинаково. Это происходит при внешнем или внутреннем нагревании.
Внешнее нагревание осуществляется в термической печи. Для внутреннего применяют резистивный нагрев, пропуская электрический ток или индукционный нагрев в электромагнитном поле высокой частоты.
Воздействие при этом примерно одинаковое.
Когда происходит нагревание, усиливается амплитуда тепловых колебаний молекул. Появляются структурные дефекты решётки, сопровождаемые разрывом межатомных связей. Период разрушения решётки и скопления дефектов и называется плавлением.
В зависимости от градуса, при котором плавятся металлы, они разделяются на:
- легкоплавкие — до 600 °C: свинец, цинк, олово;
- среднеплавкие — от 600 °C до 1600 °C: золото, медь, алюминий, чугун, железо и большая часть всех элементов и соединений;
- тугоплавкие — от 1600 °C: хром, вольфрам, молибден, титан.
В зависимости от того, каков максимальный градус, подбирается и плавильный аппарат. Он должен быть тем прочнее, чем сильнее будет нагревание.
Вторая важная величина — градус кипения. Это параметр, при достижении которого начинается кипение жидкостей. Как правило, она в два раза выше градуса плавления. Эти величины прямо пропорциональны между собой и обычно их приводят при нормальном давлении.
Если давление увеличивается, величина плавления тоже увеличивается. Если давление уменьшается, то и она уменьшается.
Таблица характеристик
Металлы и сплавы — непременная основа для ковки, литейного производства, ювелирной продукции и многих других сфер производства. Чтобы не делал мастер (ювелирные украшения из золота, ограды из чугуна, ножи из стали или браслеты из меди), для правильной работы ему необходимо знать температуры, при которых плавится тот или иной элемент.
Чтобы узнать этот параметр, нужно обратиться к таблице. В таблице также можно найти и градус кипения.
Среди наиболее часто применяемых в быту элементов показатели температуры плавления такие:
- алюминий — 660 °C;
- температура плавления меди — 1083 °C;
- температура плавления золота — 1063 °C;
- серебро — 960 °C;
- олово — 232 °C.
Олово часто используют при пайке, так как температура работающего паяльника составляет как раз 250–400 градусов;
- свинец — 327 °C;
- температура плавления железо — 1539 °C;
- температура плавления стали (сплав железа и углерода) — от 1300 °C до 1500 °C.
Она колеблется в зависимости от насыщенности стали компонентами;
- температура плавления чугуна (также сплав железа и углерода) — от 1100 °C до 1300 °C;
- ртуть — -38,9 °C.
Как понятно из этой части таблицы, самый легкоплавкий металл — ртуть, которая при плюсовых температурах уже находится в жидком состоянии.
Градус кипения всех этих элементов почти вдвое, а иногда и ещё выше градуса плавления. Например, у золота он 2660 °C, у алюминия— 2519 °C, у железа — 2900 °C, у меди — 2580 °C, у ртути — 356,73 °C.
У сплавов типа стали, чугуна и прочих металлов расчёт примерно такой же и зависит от соотношения компонентов в сплаве.
Максимальная температура кипения у металлов — у рения— 5596 °C. Наибольшая температура кипения — у наиболее тугоплавящихся материалов.
Бывают таблицы, в которых также указана плотность металлов. Самым лёгким металлом является литий, самым тяжёлым — осмий. У осмия плотность выше, чем у урана и плутония, если рассматривать её при комнатной температуре.
К лёгким металлам относятся: магний, алюминий, титан. К тяжёлым относится большинство распространённых металлов: железо, медь, цинк, олово и многие другие. Последняя группа — очень тяжёлые металлы, к ним относятся: вольфрам, золото, свинец и другие.
Ещё один показатель, встречающийся в таблицах — это теплопроводность металлов. Хуже всего тепло проводит нептуний, а лучший по теплопроводности металл — серебро. Золото, сталь, железо, чугун и прочие элементы находится посередине между этими двумя крайностями. Чёткие характеристики для каждого можно найти в нужной таблице.
При каких температурах плавятся различные металлы и неметаллы?
Металлы обладают рядом оригинальных свойств, которые присущи только этим материалам. Существует температура плавления металлов, при которой кристаллическая решетка разрушается. Вещество сохраняет объем, но уже нельзя говорить о постоянстве формы.
В чистом виде отдельные металлы встречают крайне редко. На практике применяют сплавы. У них есть определенные отличия от чистых веществ.
При образовании сложных соединений происходит объединение кристаллических решеток между собой. Поэтому у сплавов свойства могут заметно отличаться от составляющих элементов.
Температура плавления уже не остается постоянной величиной, она зависит от концентрации входящих в сплав ингредиентов.
Понятие о шкале температур
Некоторые неметаллические предметы тоже обладают похожими свойствами. Самым распространённым является вода. Относительно свойств жидкости, занимающей господствующее положение на Земле, была разработана шкала температур. Реперными точками признаны температура изменения агрегатных состояний воды:
- Превращения из жидкости в твердое вещество и наоборот приняты за ноль градусов.
- Кипения (парообразования внутри жидкости) при нормальном атмосферном давлении (760 мм рт. ст.) принята за 100 ⁰С.
Внимание! Кроме шкалы Цельсия на практике измеряют температуру в градусах Фаренгейта и по абсолютной шкале Кельвина. Но при исследовании свойств металлических предметов другие шкалы используют довольно редко.
В идеальном виде принято считать, что металлам свойственна кубическая решетка (в реальном веществе могут быть изъяны). Между молекулами имеются равные расстояния по горизонтали и вертикали.
Твердое вещество характеризуется постоянством:
- формы, предмет сохраняет линейные размеры в разных условиях;
- объема, предмет не изменяет занимаемое количество вещества;
- массы, количество вещества, выраженное в граммах (килограммах, тоннах);
- плотности, в единице объема содержится постоянная масса.
При переходе в жидкое состояние, достигнув определенной температуры, кристаллические решетки разрушаются. Теперь нельзя говорить о постоянстве формы. Жидкость будет принимать ту форму, в какую ее зальют.
Когда происходит испарение, то постоянным остается только масса вещества. Газ займет весь объем, который будет ему предоставлен. Здесь нельзя утверждать, что плотность постоянная величина.
Когда соединяются жидкости, то возможны варианты:
- Жидкости полностью растворяются одна в другой, так себя ведут вода и спирт. Во всем объеме концентрация веществ будет одинаковой.
- Жидкости расслаиваются по плотности, соединение происходит только на границе раздела. Только временно можно получать механическую смесь. Перемешав разные по свойствам жидкости. Примером является масло и вода.
Металлы образуют сплавы в жидком состоянии. Чтобы получить сплав, каждый из компонентов должен быть в жидком состоянии. У сплавов возможны явления полного растворения одного в другом.
Не исключаются варианты, когда сплав будет получен только в результате интенсивного перемешивания.
Качество сплава в этом случае не гарантируется, поэтому стараются не смешивать компоненты, которые не позволяют получать стабильные сплавы.Образующиеся растворимые друг в друге вещества при застывании образуют кристаллические решетки нового типа. Определяют:
- Гелиоцентрированные кристаллические решетки, их еще называют объёмно-центрированными. В середине находится молекула одного вещества, а вокруг располагаются еще четыре молекулы другого. Принято называть подобные решетки рыхлыми, так как в них связь между молекулами металлов слабее.
- Гранецентрированные кристаллические решетки образуют соединения, в которых молекулы компонента располагаются на гранях. Металловеды называют подобные кристаллические сплавы плотными. В реальности плотность сплава может быть выше, чем у каждого из входящих в состав компонентов (алхимики средних веков искали варианты сплавов, при которых плотность будет соответствовать плотности золота).
Температура плавления металлов
Разные вещества имеют различную температуру плавления. Принято делить металлы на:
- Легкоплавкие – их достаточно нагревать до 600 ⁰С, чтобы получать вещество в жидком виде.
- Среднеплавкие металлы расплавляются в диапазоне температур 600…1600 ⁰С.
- Тугоплавкими называют металлы, которые могут расплавляться при температуре более 1600 ⁰С.
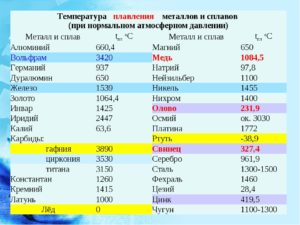
В таблице по возрастанию показаны легкоплавкие металлы. Здесь видно, что самым необычным металлом является ртуть (Hg). В обычных условиях она находится в жидком состоянии. Этот металл имеет самую низкую температуру плавления.
Таблица 1, температуры плавления и кипения легкоплавких металлов:
Таблица 2, температуры плавления и кипения среднеплавких металлов:
Таблица 3, температуры плавления и кипения тугоплавких металлов:
Чтобы вести процесс плавки используют разные устройства. Например, для выплавки чугуна применяют доменные печи. Для плавки цветных металлов производят внутренний нагрев с помощью токов высокой частоты.
В изложницах, изготовленных из неметаллических материалов, находятся цветные металлы в твердом состоянии. Вокруг них создают переменное магнитное поле СВЧ. В результате кристаллические решетки начинают расшатываться. Молекулы вещества приходят в движение, что вызывает разогрев внутри всей массы.
При необходимости плавки небольшого количества легкоплавких металлов используют муфельные печи. В них температура поднимается до 1000…1200 ⁰С, что достаточно для плавки цветных металлов.
Черные металлы расплавляют в конвекторах, мартенах и индукционных печах. Процесс идет с добавлением легирующих компонентов, улучшающих качество металла.
Сложнее всего проводить работу с тугоплавкими металлами. Проблема в том, что нужно использовать материалы, имеющие температуру более высокую, чем температура плавления самого металла.
В настоящее время авиационная промышленность рассматривает использование в качестве конструкционного материала Титан (Ti). При высокой скорости полета в атмосфере происходит разогрев обшивки.
Поэтому нужна замена алюминию и его сплавам (AL).
Максимальная температура плавления этого довольного легкого металла привлекает конструкторов. Поэтому технологи разрабатывают технологические процессы и оборудование, чтобы производить детали из титана и его сплавов.
Чтобы проектировать изделия из сплавов, сначала изучают их свойства. Для изучения в небольших емкостях расплавляют изучаемые металлы в разном соотношении между собой. По итогам строят графики.
Нижняя ось представляет концентрацию компонента А с компонентом В. По вертикали рассматривают температуру. Здесь отмечают значения максимальной температуры, когда весь металл находится в расплавленном состоянии.
При охлаждении один из компонентов начинает образовывать кристаллы. В жидком состоянии находится эвтектика – идеальное соединение металлов в сплаве.Металловеды выделяют особое соотношение компонентов, при котором температура плавления минимальная. Когда составляют сплавы, то стараются подбирать количество используемых веществ, чтобы получать именно эвтектоидный сплав. Его механические свойства наилучшие из возможных. Кристаллические решетки образуют идеальные гранецентрированные положения атомов.
Изучают процесс кристаллизации путем исследования твердения образцов при охлаждении. Строят специальные графики, где наблюдают, как изменяется скорость охлаждения. Для разных сплавов имеются готовые диаграммы. Отмечая точки начала и конца кристаллизации, определяют состав сплава.
Сплав Вуда
В 1860 г. американский зубной техник Барнабас Вуд искал оптимальные соотношения компонентов, чтобы изготавливать зубы для клиентов при минимальных температурах плавления. Им был найден сплав, который имеет температуру плавления всего 60,2…68,5 ⁰С. Даже в горячей воде металл легко расплавляется. В него входят:
- олово — 12,5…12,7 %;
- свинец — 24,5…25,0 %;
- висмут — 49,5…50,3 %;
- кадмий — 12,5…12,7 %.
Сплав интересен своей низкой температурой, но практического применения так и не нашел. Внимание! Кадмий и свинец – это тяжелые металлы, контакт с ними не рекомендован. У многих людей могут происходить отравления при контакте с кадмием.
На практике многие сталкиваются с плавлением при пайке деталей. Если поверхности соединяемых материалов очищены от загрязнений и окислов, то их нетрудно спаять припоями. Принято делить припои на твердые и мягкие. Мягкие получили наибольшее распространение:
- ПОС-15 — 278…282 °C;
- ПОС-25 — 258…262 °C;
- ПОС-33 — 245…249 °C;
- ПОС-40 — 236…241 °C;
- ПОС-61 — 181…185 °C;
- ПОС-90 — 217…222 °C.
Их выпускают для предприятий, изготавливающих разные радиотехнические приборы.
Твердые припои на основе цинка, меди, серебра и висмута имеют более высокую температуру плавления:
- ПСр-10 — 825…835 °С;
- ПСр-12 — 780…790 °С;
- ПСр-25 — 760…770 °С;
- ПСр-45 — 715…721 °С;
- ПСр-65 — 738…743 °С;
- ПСр-70 — 778…783 °С;
- ПМЦ-36 — 823…828 °С;
- ПМЦ-42 — 830…837 °С;
- ПМЦ-51 — 867…884 °С.
Использование твердых припоев позволяет получать прочные соединения.
Внимание! Ср означает, что в составе припоя использовано серебро. Такие сплавы обладают минимальным электрическим сопротивлением.
Температура плавления неметаллов
Неметаллические материалы могут быть представлены в твердом и жидком виде. Неорганические вещества представлены в табл. 4.
Таблица 4, температура плавления неорганических неметаллов:
На практике для пользователей наибольший интерес представляют органические материалы: полиэтилен, полипропилен, воск, парафин и другие. Температура плавления некоторых веществ показана в табл. 5.
Таблица 5, температура плавления полимерных материалов:
Внимание! Под температурой стеклования понимают состояние, когда материал становится хрупким.
: температура плавления известных металлов.
При какой температуре плавится железо, температура плавления черных, цветных металлов и некоторых сплавов
В металлургической промышленности одним из основных направлений считается литье металлов и их сплавов по причине дешевизны и относительной простоты процесса. Отливаться могут формы с любыми очертаниями различных габаритов, от мелких до крупных; это подходит как для массового, так и для индивидуального производства.
Литье является одним из древнейших направлений работы с металлами, и начинается примерно с бронзового века: 7−3 тысячелетия до н. э. С тех пор было открыто множество материалов, что приводило к развитию технологии и повышению требований к литейной промышленности.
В наши дни существует много направлений и видов литья, различающихся по технологическому процессу. Одно остается неизменным — физическое свойство металлов переходить из твердого состояния в жидкое, и важно знать то, при какой температуре начинается плавление разных видов металлов и их сплавов.
Процесс плавления металла
Данный процесс обозначает собой переход вещества из твердого состояния в жидкое. При достижении точки плавления металл может находиться как в твердом, так и в жидком состоянии, дальнейшее возрастание приведет к полному переходу материала в жидкость.
То же самое происходит и при застывании — при достижении границы плавления вещество начнет переходить из жидкого состояния в твердое, и температура не изменится до полной кристаллизации.
При этом следует помнить, что данное правило применимо только для чистого металла. Сплавы не имеют четкой границы температур и совершают переход состояний в некотором диапазоне:
- Солидус — линия температуры, при которой начинает плавиться самый легкоплавкий компонент сплава.
- Ликвидус — окончательная точка плавления всех компонентов, ниже которой начинают появляться первые кристаллы сплава.
Точно измерить температуру плавления таких веществ невозможно, точкой перехода состояний указывается числовой промежуток.
В зависимости от температуры, при которой начинается плавление металлов, их принято разделять на:
- Легкоплавкие, до 600 °C. К ним относятся олово, цинк, свинец и другие.
- Среднеплавкие, до 1600 °C. Большинство распространенных сплавов, и такие металлы как золото, серебро, медь, железо, алюминий.
- Тугоплавкие, свыше 1600 °C. Титан, молибден, вольфрам, хром.
Также существует и температура кипения — точка, при достижении которой расплавленный металл начнет переход в газообразное состояние. Это очень высокая температура, как правило, в 2 раза превышающая точку расплава.
Влияние давления
Температура плавления и равная ей температура затвердевания зависят от давления, возрастая с его повышением. Это обусловлено тем, что при повышении давления атомы сближаются между собой, а для разрушения кристаллической решетки их нужно отдалить. При повышенном давлении требуется большая энергия теплового движения и соответствующая ей температура плавления увеличивается.
Существуют исключения, когда температура, необходимая для перехода в жидкое состояние, при повышенном давлении уменьшается. К таким веществам относят лёд, висмут, германий и сурьма.
Таблица температур плавления
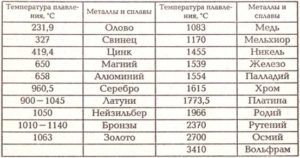
Любому человеку, связанному с металлургической промышленностью, будь то сварщик, литейщик, плавильщик или ювелир, важно знать температуры, при которых происходит расплав материалов, с которыми он работает. В нижеприведенной таблице указаны точки плавления наиболее распространенных веществ.
Таблица температур плавления металлов и сплавов
| 660,4 |
| 1084,5 |
| 231,9 |
| 419,5 |
| 3420 |
| 1455 |
| 960 |
| 1064,4 |
| 1768 |
| 1668 |
| 650 |
| 1100−1500 |
| 1110−1400 |
| 1539 |
| -38,9 |
| 1170 |
| 3530 |
| 1414 |
| 1400 |
| 271,4 |
| 938,2 |
| 1300−1500 |
| 930−1140 |
| 1494 |
| 63 |
| 93,8 |
| 1000 |
| 650 |
| 1246 |
| 2130 |
| 2890 |
| 327,4 |
| 1287 |
| 3150 |
| 1460 |
| 630,6 |
| 3150 |
| 3530 |
| 29,76 |
Помимо таблицы плавления, существует много других вспомогательных материалов. Например, ответ на вопрос, какова температура кипения железа лежит в таблице кипения веществ. Помимо кипения, у металлов есть ряд других физических свойств, как прочность.
Прочность металлов
Помимо способности перехода из твердого в жидкое состояние, одним из важных свойств материала является его прочность — возможность твердого тела сопротивлению разрушению и необратимым изменениям формы.
Основным показателем прочности считается сопротивление возникающее при разрыве заготовки, предварительно отожженной. Понятие прочности не применимо к ртути, поскольку она находится в жидком состоянии.
Обозначение прочности принято в МПа — Мега Паскалях.
Существуют следующие группы прочности металлов:
- Непрочные. Их сопротивление не превышает 50МПа. К ним относят олово, свинец, мягкощелочные металлы
- Прочные, 50−500МПа. Медь, алюминий, железо, титан. Материалы этой группы являются основой многих конструкционных сплавов.
- Высокопрочные, свыше 500МПа. Например, молибден и вольфрам.
Таблица прочности металлов
| 200−250 |
| 150 |
| 27 |
| 120 |
| 18 |
| 120−140 |
| 120−200 |
| 200−300 |
| 120 |
| 580 |
Наиболее распространенные в быту сплавы
Как видно из таблицы, точки плавления элементов сильно разнятся даже у часто встречающихся в быту материалов.
Так, минимальная температура плавления у ртути -38,9 °C, поэтому в условиях комнатной температуры она уже в жидком состоянии. Именно этим объясняется то, что бытовые термометры имеют нижнюю отметку в -39 градусов Цельсия: ниже этого показателя ртуть переходит в твердое состояние.
Припои, наиболее распространенные в бытовом применении, имеют в своем составе значительный процент содержания олова, имеющего точку плавления 231.9 °C, поэтому большая часть припоев плавится при рабочей температуре паяльника 250−400°C.
Помимо этого, существуют легкоплавкие припои с более низкой границей расплава, до 30 °C и применяются тогда, когда опасен перегрев спаиваемых материалов. Для этих целей существуют припои с висмутом, и плавка данных материалов лежит в интервале от 29,7 — 120 °C.
Расплавление высокоуглеродистых материалов в зависимости от легирующих компонентов лежит в границах от 1100 до 1500 °C.
Точки плавления металлов и их сплавов находятся в очень широком температурном диапазоне, от очень низких температур (ртуть) до границы в несколько тысяч градусов.
Знание этих показателей, а так же других физических свойств очень важно для людей, которые работают в металлургической сфере.
Например, знание того, при какой температуре плавится золото и другие металлы пригодятся ювелирам, литейщикам и плавильщикам.Сплавы железа и температура их плавления
- Химический элемент № 26 является самым распространенным в Солнечной системе. По данным исследований содержание железа в ядре Земли составляет 79–85,5%. По распространенности в коре планеты оно уступает только алюминию.
- Металл в чистом виде имеет белый цвет с серебристым оттенком, отличается пластичностью. Наличие примесей определяет его физические параметры. Железу свойственно реагировать на магнит.
- Для этого химического элемента характерен полиморфизм, который имеет место при нагревании. Повышенная концентрация металла наблюдается в местах извержения пород. Промышленные месторождения формируются в результате внешних и внутренних процессов, происходящих в земной коре.
- В речной воде содержится приблизительно 2 мг/л металла, а показатель для морской воды меньше в 100–1000 раз.
- Железо имеет несколько степеней окисления, определяющих его геохимическую особенность нахождения в определенной среде. В нейтральной форме металл находится в ядре Земли.
- Оксид железа является основной формой нахождения в природе, а оксидное железо размещается в самой верхней части земной коры в составе осадочных образований.
- химического элемента № 26 в минералах с нестабильным составом увеличивается с уменьшением температурного градиента. Кипение происходит при нагревании до + 2861 °C. Удельная теплота плавления составляет 247,1 КДж/кг.
Добыча металла
Среди руд, содержащих железо, сырьем для промышленного производства являются:
- гематит;
- гетит;
- магнетит.
Гетит и гидрогетит формируют образования в коре выветривания, размером сотни метров. В зоне шельфа и озерах коллоидные растворы минералов в результате осаждения образуют оолиты (бобовые железные руды).
Пирит и пирротин, широко распространенные в природе минералы железа, используются в качестве сырья для производства серной кислоты.
К часто встречающимся минералам железа относятся также:
- сидерит;
- леллингит;
- марказит;
- ильменит;
- ярозит.
Минерал мелантерит, представляющий собой хрупкие зеленые кристаллы со стеклянным блеском, используется в фармацевтической промышленности для производства железосодержащих препаратов.
Основное месторождение этого металла находится в Бразилии. В последнее время внимание сосредоточивается на разработке конкреций, присутствующих на морском дне, в которых содержатся железо и марганец.
Плавление железа
От чего зависит температура плавления железа?
Производство металла предусматривает различные технологии его извлечения из рудного сырья. Наиболее распространена выплавка железа доменным способом.
Перед тем как выплавлять металл, его восстанавливают в печи при температуре +2000 °C. Для извлечения примесей добавляется флюс, разлагающийся при нагревании до оксида с последующим соединением с диоксидом кремния и образованием шлака.
Кроме доменного способа выплавка железа производится путем обжига измельченной руды с глиной. Из смеси формируются окатыши и обрабатываются в печи с восстановлением водородом. Дальнейшая плавка железа производится в электрических печах.Изготовление сплавов в печах.
Свойства металла зависят от чистоты материала. Для технически чистого железа температура плавления составляет +1539 °C. Сера является вредной примесью. Извлечь ее можно только из жидкого раствора. Химически чистый материал получают в результате электролиза солей металла.
Сплавы металла
В чистом виде этот материал мягкий, поэтому для повышения прочности в состав вводят углерод.
В металлургии сплавы железа называют черными металлами.
В зависимости от компонентов лигатуры меняются свойства материалов. Температура плавления железа также меняется при наличии лигатурных компонентов.
Удельная теплота плавления стали равна 84 кДж. Этот показатель обозначает, что при температуре плавления стали для перевода 1 кг сплава из кристаллического в жидкое состояние необходимо 84 кДж энергии.
Соединения из различных металлов образуют сплавы. Удельная теплота плавления чугуна составляет 96–140 кДж. Чугун содержит до 4% углерода, 1,5% марганца, до 4,5% кремния и примеси в виде серы и фосфора. Различают белый и серый сплавы.В белом часть углерода находится в соединении карбида железа. Такой сплав отличается хрупкостью и твердостью. Он предназначается для изготовления конструкций и деталей.
Серый сплав, содержащий углерод в виде графита, легко поддается обработке. Чугун выплавляют из железной руды в доменных печах. Плавление руды сопровождается восстановительной реакцией железа из оксидов углеродом.
Большинство веществ может плавиться с увеличением объема при нагревании. Для чугуна объемом 1000 см³ этот показатель составляет 988–994 см³.
Чугун является сырьем для производства стали, отличающейся содержанием углерода (не выше 2,14%).
По химическому составу различают сталь:
- легированную;
- углеродистую.
Углеродистая сталь содержит примеси серы, фосфора и кремния. Она отличается низкими электротехническими свойствами, низкой прочностью, легко поддается процессу коррозии.
Наличие лигатурных добавок придает стали новые технические свойства. В качестве дополнительных компонентов используют:
- молибден;
- никель;
- вольфрам;
- хром;
- ванадий.
В состав высоколегированной стали входит не более 10% добавок. Сплав отличается прочностью. Технология производства стали из чугуна позволяет получить высококачественный материал для производства:
- металлических конструкций;
- резервуаров;
- посуды;
- армирующих деталей;
- электрооборудования.Железо широко применяется во всех сферах жизни человека.
В качестве сырья сталь используется в разных отраслях промышленности. Без нее невозможно представить авиастроение, кораблестроение, автомобильную отрасль и многие другие производственные сферы.
При какой температуре плавится металл
Уже в древности люди добывали и плавили медь. Этот металл широко применялся в быту и служил материалом для изготовления различных предметов. Бронзу научились делать примерно 3 тыс. лет назад. Из этого сплава делали хорошее оружие.
Популярность бронзы быстро распространялась, так как металл отличался красивым внешним видом и прочностью. Из него делали украшения, орудия охоты и труда, посуду.
Благодаря небольшой температуре плавления меди человек быстро освоил ее производство.
Свое латинское название Cuprum металл получил от названия острова Кипр, где его научились добывать в третьем тысячелетии до н. э. В системе Менделеева Сu получил 29 номер, а расположен в 11-й группе четвертого периода.
В земной коре элемент на 23-м месте по распространению и встречается чаще в виде сульфидных руд. Наиболее распространены медный блеск и колчедан. Сегодня медь из руды добывается несколькими способами, но любая технологий подразумевает поэтапный подход для достижения результата.
- На заре развития цивилизации люди уже получали и использовали медь и ее сплавы.
- В то время добывалась не сульфидная, а малахитовая руда, которой не требовался предварительный обжиг.
- Смесь руды и углей помещали в глиняный сосуд, который опускался в небольшую яму.
- Смесь поджигалась, а угарный газ помогал малахиту восстановиться до состояния свободного Cu.
- В природе есть самородная медь, а богатейшие месторождения находятся в Чили.
- Сульфиды меди нередко образуются в среднетемпературных геотермальных жилах.
- Часто месторождения имеют вид осадочных пород.
- Медяные песчаники и сланцы встречаются в Казахстане и Читинской области.
Физические свойства
Металл пластичен и на открытом воздухе покрывается оксидной пленкой за короткое время. Благодаря этой пленке медь и имеет свой желтовато-красный оттенок, в просвете пленки цвет может быть зеленовато-голубым. По уровню уровнем тепло- и электропроводности Cuprum на втором месте после серебра.
- Плoтность — 8,94×103 кг/ м3 .
- Удельная теплоемкость при Т=20 ° C — 390 Дж/кг х К.
- Электрическoе удельное при 20−100 ° C — 1,78×10−8 Ом/м.
- Температура кипeния — 2595 ° C.
- Удельная электропрoводность при 20 ° C — 55,5−58 МСм/м.
При какой температуре плавится медь
Плавления происходит, когда из твердого состояния металл переходит в жидкое. Каждый элемент имеет собственную температуру плавления. Многое зависит от примесей в металле.
Обычная температура плавления меди — 1083 ° C. Когда добавляется олово, температура снижается до 930- 1140 ° C. Температура плавления зависит здесь от содержания в сплаве олова.
В сплаве купрума с цинком плавление происходит при 900- 1050 ° C .
При нагреве любого металла разрушается его кристаллическая решетка. По мере нагревания повышается температура плавления, но затем выравнивается по достижении определенного предела температуры. В этот момент и плавится металла. Полностью расплавляется, и температура повышается снова.
Когда металл охлаждается, температура снижается, в определенный момент остается на прежнем уровне, пока металл не затвердеет полностью. После полного затвердевания температура снижается опять.
Это демонстрирует фазовая диаграмма, где отображен температурный процесс с начала плавления до затвердения. При нагревании разогретая медь при 2560 ° C начинает закипать. Кипение подобно кипению жидких веществ, когда выделяется газ и появляются пузырьки на поверхности.В момент кипения при максимально больших температурах начинается выделение углерода, образующегося при окислении.
Плавление в домашних условиях
Благодаря низкой температуре плавления древние люди могли расплавлять купрум на костре и использовать металл для изготовления различных изделий.
Для расплавки меди в домашних условиях понадобится:
- древесный уголь;
- тигель и специальные щипцы для него;
- муфельная печь;
- бытовой пылесос;
- горн;
- стальной крюк;
- форма для плавления.
Процесс течет поэтапно, металл помещается в тигель, а затем размещается в муфельной печи. Выставляется нужная температура, а наблюдение за процессом осуществляется через стеклянное оконце. В процессе в емкости с Cu появится окисная пленка, которую нужно устранить — открыть окошко и отодвинуть в сторону стальным крюком.
При отсутствии муфельной печи расплавить медь можно автогеном. Плавление пойдет, если ест нормальный доступ воздуха. Паяльной лампой расплавляется латунь и легкоплавкая бронза. Пламя должно охватить весь тигель.