Как бороться с коррозией металла
Коррозия — это? Виды и способы защиты от коррозии на металлических изделиях
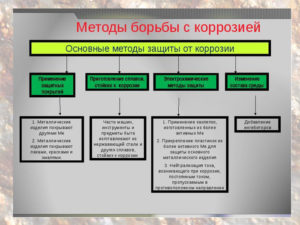
Коррозия металла – это ржавчина, в первую очередь, которая образовалась на поверхности, чем больше ржавчины, тем глубже она проникает и разрушает материал элемента.
Любую коррозию возможно охарактеризовать тремя признаками:
- Во-первых, это восстановительно-окислительный процесс.
- Во-вторых, этот процесс является самопроизвольным, то есть возникает в любых условиях.
- В-третьих, процесс коррозии чаще всего возникает и распространяется на поверхности элемента, и иногда проникает вглубь.
Коррозия металла — это процесс, который проходит в химических или электрохимических средах, он приводит к повреждению верхних слоев материала.
Коррозии поддаются не только металлические изделия, но и бетонные, а также керамические.
Виды коррозии по характеру разрушения
На материале может протекать коррозия двух видов:
- Сплошная – распространена на всей поверхности изделия. Такой вид также делится на несколько подвидов:
- Равномерная – ржавчина появляется в одинаковом количестве на всех участках изделия.
- Неравномерная – ржавчина появляется с разной скоростью на разных участках.
- Избирательная – разрушению подвергается определенный компонент металлического сплава.
- Местная – коррозия образуется на отдельных небольших по размеру участках на поверхности детали. Выражается в единичных углублениях, раковинах и коррозирующих точках.
Виды коррозии металлов по механизму протекания
Существует несколько причины возникновения коррозии металла, химия этих процессов на сегодняшний день достаточно изучена, что помогает эффективно бороться с разрушением материалов.
Химическая коррозия металлов – происходит между металлом и средой, протекает окислительно-восстановительная реакция. Данный вид коррозии характерен для такой среды, в который не может протекать электрический ток. Химическая коррозия по условию протекания может быть:
- При газовой коррозии ржавчина возникает в результате воздействия на металл газовой среды чаще всего при высоких температурах. Особенностью этого вида является то, что воздействие газовой среды на некоторые металлы приводит к их полному разрушению, но на некоторых металлах (цирконий, алюминий, хром) протекающая реакция оставляет лишь защитную пленку.
- Жидкостная поверхностная коррозия возникает при воздействии жидких агрессивных сред, также без возможности протекания электрического тока.
Электрохимическая коррозия – эта реакция имеет место быть только в средах, где возможно протекание электрического тока.
Электрохимическая коррозия имеет возможность протекать в самых разных средах, но все они делятся на два типа по условию протекания:
- Коррозия с участим электролитов в растворах– протекает в среде кислот, соли, воде, оснований.
- Коррозия в атмосферных условиях – является самой часто встречающейся коррозией.
Виды коррозии по условиям протекания
Как было отмечено выше, по условиям протекания коррозия может быть газовой, жидкостной, атмосферной или в растворах электролитов. Необходимо сделать этот список более полным, поэтому ниже раскрыты дополнительные типы коррозии:
- Коррозия металлов, протекающая в почвах и грунтах;
- Биокоррозия, возникающая вследствие жизнедеятельности микроорганизмов на поверхности материала;
- Структурная — возникает из-за неоднородной структуры металла;
- Контактная коррозия проявляется при долгом соприкосновении металлов с различными потенциалами в электролите;
- Трение материала в коррозийной среде;
- Коррозия, возникающая от трения материала в коррозийной среде;
- Фреттинг-коррозия проявляется во время возникновения колебаний в коррозийной среде;
- Кавитация появляется при воздействии существующей коррозийной среды и ударного воздействия извне.
Результат коррозии
Пластинчатая коррозия металла – вид на протекающий процесс
Основные типы атмосферной коррозии
Принято выделять три основных типа атмосферной коррозии: влажная, мокрая, сухая. Жидкая и мокрая, в силу способности проводить электрический ток, протекают по электрохимическим законам, а сухая по химическим.
- Влажная глубокая коррозия металла будет протекать там, где на металле можно наблюдать тонкую влажную пленку. В зависимости от происходящего в окружающей среде, на пленке может образовываться конденсат, после чего начинается процесс коррозийного разрушения.
- Мокрая коррозия начинается на поверхности хорошо увлажненной, при относительной влажности окружающей среды около 100%. Капли, образовавшиеся на поверхности, помогают коррозийному износу.
- Сухая атмосферная коррозия менее агрессивна, потому что процесс разрушения протекает при малой влажности воздуха. Образовавшаяся на изделии пленка замедляет образование ржавчины.
Закорродировавший корабль
Виды коррозии бетона
Бетон является крепким каменным строительным материалом, состоящим из цемента, наполнителя и связующих веществ. Так как этот материал эксплуатируется в условиях открытой окружающей среды, а также нередко в агрессивно-опасных средах, то он так же подвержен коррозийному износу.
Схема коррозии на бетоне
Существует несколько видов бетонной коррозии:
- В результате взаимодействия с окружающей средой, на поверхности бетона могут образовываться легкорастворимые соли, которые при взаимодействии с внутренними компонентами материала приводят к его разрушению.
- Часто встречающаяся проблема – это разъединение составных частей цементного камня водой или вымывание гидроксида кальция, который образовывается в процессе такой реакции или ранее.
- В условиях окружающей среды, в состав бетона проникают вещества, которые имеют достаточно большой объем, в сравнении с исходными продуктами реакции, что приводит к механическим и химическим повреждениям целостности материала, далее эти участки под воздействием окружающей среды начинают коррозировать про принципу 1 или 2.
При коррозии бетона, невозможно выявить только одну причину, зачастую образовавшаяся коррозия – продукты нескольких факторов в совокупности.
Коррозия железа
Давно выявлено, что зачастую коррозия (ржавчина) на железных элементах возникает вследствие протекания реакций окисления воздухом или кислотами – окислительно-восстановительные реакции. Как и в любом металле, ржавчина захватывает верхние слои железного изделия и возникает химическая коррозия, электрохимическая или электрическая.
Если рассмотреть каждый этот процесс в отдельности то получится, что при химическом возникновении ржавчины происходит переход электронов на окислитель, в результате образовывается оксидная пленка, а реакция выглядит так:
3Fe + 2O2 = Fe3O4 (FeO•Fe2O3)
Образовавшаяся пленка не защищает материал от дальнейшего возникновения окислительно-восстановительных реакций, она свободно пропускает воздух, что способствует образованию новой ржавчины.
При электрохимической коррозии, которая чаще всего возникает с железом в грунте, протекает реакция с образованием свободного кислорода и воды, если они остаются на железном элементе, то это вызывает новые продукты коррозии.Fe + O2 + H2O → Fe2O3 · xH2O
Электрическая коррозия железа является самой непредсказуемой, так как возникает из-за блуждающих токов, которые могут попадать к железному элементу от линий электропередач, трамвайных путей, крупногабаритного электрооборудования и другое. Блуждающий ток запускает процесс электролиза металла, а он способствует образованию ржавых пятен.
Коррозия меди
При эксплуатации медных элементов необходимо учитывать причины коррозии, зачастую они обусловлены средой, где находится элемент. Например, в таких средах как: атмосферная, морская вода, при контакте с галогеновыми веществами и в слабых растворах солей медь коррозирует стабильно медленно.
1)Cu+2H2SO4→CuSO4+SO2↑+2H2O
2)Cu+H2SO4→CuO+SO2↑+H2O
Также медь подвергается коррозии в обычных атмосферных условиях:
2Cu+H2O+CO2+O2→ CuCO3*Cu(OH)2
Методы и способы защиты металлов от коррозии
Вследствие того, что коррозийный процесс протекает на верхних слоях металла конструкции, то защита поверхности заключается в создании верхнего защитного слоя для изделия, который убирает следы коррозии на металле. Такими защитными покрытиями выступают вещества металлические и неметаллические.
Важно понимать, что защита от коррозии не избавляет от нее, а лишь замедляет уже происходящие процессы. Однако, если верно подобрать средство борьбы, то возможно замедлить процесс образования коррозии на несколько лет.
Исходя из названия, металлические покрытия – это вещества, в основе которых металл. Например, чтобы защитить конструкцию из железа от коррозии на ее поверхность наносят слои цинка, меди или никеля.
Очистка труб от коррозии
Неметаллические покрытия – специальные вещества, наиболее широкая группа защитных соединений. Они изготавливаются в виде красок, эмалей, смазок, грунтовок, составов на битумной и битумно-полимерной основе и т.д.
Большая популярность неметаллических соединений в устранении следов коррозии заключается в их широком выборе, большом ценовом диапазоне, легкости изготовления и хороших защитных свойствах.
Наименьшую популярность приобрели химические покрытия из-за необходимости проводить сложные химические процессы:
- Оксидирование – образование оксидных пленок на поверхностях защищаемых деталей.
- Азотирование – насыщение верхних слоев материала азотом.
- Цементация – реакция, при которой верхние слои соединяются с углеродом и т.д.
Также при коррозии металлов существуют способы защиты, при которых на этапе сплавления металлов в них вводят специальные соединения, которые смогут повысить коррозийную устойчивость будущего материала.
Большую группу защиты представляют способы электрохимической и протекторной защиты.
Электрохимическая защита состоит в процессе преобразования продуктов коррозии в среде электролитов с помощью проводящего электрического тока. Постоянный ток присоединяется к катоду (защищаемому материалу), а в качестве анода выступает проводящий металлический источник, который при своем разрушении защищает объект от ржавчины.
Электрохимическая защита от коррозии
Протекторная защита протекает по такому же принципу, однако вместе металлического связующего изделия выступают специальные изделия – протекторы, которые выступают в роли анода. В результате протекающей реакции, протектор разрушается, защищая катод (конструкцию из металла).
Таким образом, хоть коррозия является необратимым процессом, но на данный момент люди научились эффективно замедлять ее губительное воздействие.Как бороться с коррозией металла

разрушение металла
Металл под воздействием влаги начинает разрушаться. Этот процесс получил название коррозия или ржавчина.
Особенно активно проходит коррозийное разрушение черных металлов.
Проблема состоит не в том, что металл приходит в негодность.
Производственный процесс нарушается, когда ржавчиной покрываются отдельные детали и части машин, конструкций, станков, требующие замены.
Спасти производство может только своевременная борьба с коррозией.
Как различать виды коррозии
Металл, попадающий в агрессивную среду (повышенная влажность, вода, намерзание льда и т.п.), начинает окисляться, покрываясь ржавчиной. Разрушение проходит в результате химической коррозии.
Металл, растворяющийся в жидком электролите, подвергается электрохимической коррозии.
Особенно это заметно на стыках между разными видами металлов, например, на сварочных швах.
Как бороться с коррозией
Активный способ защиты металла предполагает изменение электрического поля с целью повышения электродной стойкости материала. Можно использовать для обработки металлических изделий анод, который в процессе разрушения защищает поверхность от коррозии.
Пассивный способ рассчитан на простое покрытие поверхности лако-красочными изделиями. Эти материалы создают защитную пленку, не пропускающую агрессивные элементы к металлу.
Наносят защитные слои на поверхность по-разному. Процесс может проводиться в производственных условиях методом напыления, под воздействием высоких температур, холодным способом. В кустарных условиях пользуются щеткой, валиком или специальным распылителем красок.
Часто используют метод холодного цинкования. Холодное цинкование эффективно тем, что приостанавливает развитие коррозии, даже если верхний слой поврежден.
Используя пассивный способ, необходимо обезжиривать поверхность металла перед покраской. Для этого нужно воспользоваться механическим способом или специальными химическими средствами. Обезжиривание поверхностей разных металлических предметов зачастую требует комбинированного способа.
Конструкционный способ борьбы со ржавчиной основан на использовании различных сплавов, резиновых прокладок и т. п.
Борьба с коррозией будет результативной, если предварительно пораженные участки или металлический предмет полностью подготовить к покрытию согласно всем правилам. С поверхности удаляется ржавчина и ее остатки.
Обезжиривание проводится разными методами, в зависимости от степени поражения металла.
Не стоит забывать о специальных химических средствах — растворителях, содержащих ПАБ (поверхностно-активное вещество) и щелочные смеси. Именно такая жидкость легко снимает коррозийные налеты.
Рекомендуем
NITTRON — нейтральный преобразователь ржавчины. Предназначен для модификации коррозии на поверхностях черных металлов, строительных металлоконструкций, труб, арматурных сталей. Без кислоты.
Подробнее
DOCKER STEEL — преобразователь ржавчины. Модифицирует ржавчину в защитную пленку, обладает высокой адгезией к поверхности, идеален для обработки гаражей, крыш, заборов и решеток, металлоконструкций, оборудования, агрегатов, бочек, кузовов. Содержит ортофосфорную кислоту.
Подробнее
Как убрать ржавчину
Удалитель ржавчины
Методы борьбы с коррозией
Методов, приемов и средств борьбы с коррозией достаточно много. Как же устранить или хотя бы уменьшить коррозию? Например, коррозию можно устранить с помощью нанесения различных защитных покрытий, введением ингибиторов, таких как нитриты, хроматы, арсениты, а также применять стойкие к коррозии материалы.
Не стоит забывать о том, что каждый случай индивидуален, и нужно решать какое из средств и в каком из сочетаний его применить, что б достигнуть самого большого экономического эффекта.
На данный момент в производство вводят новые, постоянно увеличивающиеся объемы изделий из металла, и как следствие растут убытки, состоящие из миллионов тонн подверженного коррозии металла, и миллиардами рублей, которые затрачены на борьбу с ней.Все вышеперечисленные факты исследования в этой области делают важными и актуальными.
Защита металлов от разъедания строится на следующих методах:
1. увеличивать химическое сопротивление материалов конструкции;
2. изолировать поверхность металла от агрессивной среды;
3. уменьшение агрессии в среде;
4. электрохимическая защита.
Эти методы делятся на две группы.
Два первых метода чаще всего реализуются к началу эксплуатации на производстве металлического изделия (выбор материалов для конструкции и их сочетаний во время проектировки и изготовления изделия, и нанесение на него защитных покрытий).
Два последних метода могут быть реализованы лишь в процессе использования металлического изделия, необходимо пропускать через него ток, что б достичь хорошего потенциала защиты, а также внести в технологическую среду специальные добавки, и не должны быть связаны с обработкой до того времени, как начнется их использование.
В первых двух методах не нужно изменять состав стали и природу защитного покрытия изделия при постоянной его работе в условиях агрессивной среды.
Методы второй группы помогают создавать новые защитные режимы и обеспечивают минимальную коррозию при условии в изменении эксплуатации изделий.
Для примера — на различных участках трубопровода, могут поддерживаться разные плотности тока, а в зависимости от сорта нефти, которая проходит в трубах данного состава используют различные вещества, которые тормозят химическую реакцию (ингибиторы).
Основные методы борьбы с коррозией металлов
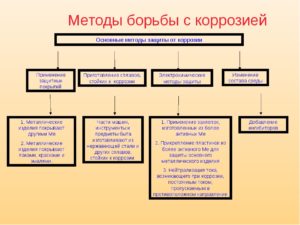
Кто знает, что в переводе с латинского означает коррозия? Это слово переводится как «грызть». Данный процесс протекает от взаимодействия металлов с окружающей средой и относится к категории химического взаимодействия.
Поэтом борьба с коррозией так актуальна в настоящее время.
Предупреждение коррозии
Разрушение металлов или коррозия металлов начинается только на поверхности и является процессом самопроизвольным.
Его нельзя ни в коем случае путать с процессом эрозия металлов, где разрушение происходит под механическим воздействием окружающей среды.
С использованием металлов в строительстве постоянно ведется борьба с коррозией металла, человечество год от года изобретает новые методы, которые помогают увеличить срок эксплуатации металлических изделий и конструкций.
Поэтому защита металлов – это основная проблема, которая до сих пор считается одной из важных составляющих в сфере строительства.
Результатом коррозии металла обычно являются продукты, связанные с окислением самого металла. А это:
- Оксиды;
- Гидроксиды;
- И так далее.
А это в свою очередь ведет к изменениям свойств, и к тому же не в лучшую сторону.
Виды процесса разрушения металлов
Коррозию металлов ученые разделили на два вида:
- Химическая коррозия металлов;
- Электрохимическая коррозия.
Первый вид коррозии еще называют газовым, это связано с тем, что часто данный процесс происходит под воздействием газовых составляющих, которые находятся в окружающей среде, но при этом высокая температура обязательный фактор.
Агрессивные среды также могут вызвать химическую коррозию металла. И все же главная отличительная черта химической коррозии – это отсутствие электрического тока в системе, где она образуется.
Продукты окисления, образующиеся на поверхности металла, служат толчком к разрушению самого металла
Ко второму виду коррозии металлов относится коррозия, где процесс разрушения происходит под воздействием электрического тока.
Здесь необходимо дать пояснения и привести примеры, которые точно раскроют процесс электрохимической коррозии металлов.
Начнем с примеров. Любые виды металлических конструкций, расположенных
- В грунтах;
- Воде морской или пресной;
- В атмосфере;
- Закрытые пленкой, где образуется влага.
Узлы и детали машин и механизмов, работающих в охлаждающих жидкостях, растворах, предназначенных для технических нужд и так далее. Это все подвержено электрохимической коррозии металлов.
Как было сказано выше, данный процесс происходит на поверхности металла. И здесь главную роль играют электроны, которые под воздействием определенных химических реакций переносятся от одной среды в другую.
Точнее сказать, между двумя веществами, одним из которых является металл, а с другой стороны выступают, к примеру, вода или грунт, образуется электрический ток, разделяющий вещества на катоды и аноды. Особенно это сильно заметно, если металл имеет примеси и различные включения, то есть масса металла является неоднородной.И здесь участки металла, разделенные примесями, создают катодные и анодные зоны, которые в свою очередь и разрушают сам металл.
Из школьного курса химии можно вспомнить один опыт, где простой стальной гвоздь, обмотанный медной проволокой, опускали в раствор поваренной соли. Через пару дней гвоздь начинал сильно ржаветь.
Опыт показывал, как происходит процесс коррозии металлов. В данном случае роль анода выполняет гвоздь, а роль катода – медная проволока.
В процессе химической реакции, а раствор поваренной соли – это прекрасный электролит, происходит передача электронов от гвоздя (железо) к меди.
Электроны в данном случае выступают в роли ионов. Перешедшие в раствор ионы двигаются к медной проволоке, где и разряжаются.
Медь набирает отрицательный потенциал, который со временем выравнивается с гвоздем. И здесь коррозия металла, в данном случае гвоздя, прекращается.
К сожалению, все металлические детали подвержены коррозии
Электрохимическая коррозия металла в основном зависит от присутствия влаги. Но, к примеру, атмосферная коррозия будет также зависеть от качества самого металла.
Трещины, шероховатость поверхности и другие дефекты будут только ускорять процесс коррозии.
А почвенная коррозия металлов сделает любой трубопровод, не защищенный специальной изоляцией, негодным. И для этого понадобится всего несколько месяцев.Ведь в почве большое количество не только влаги, но и различных химически активных элементов, которые создают повышенную кислотную среду.И сегодня защита трубопроводов – это неотъемлемая часть в строительной области.
Необходимо отметить и блуждающие токи, которые создают все условия для образования коррозии металлов. Здесь необходимо отметить:
- Линии электропередач;
- Электроустановки;
- Железная дорога, которая работает на электрическом токе;
- И так далее.
Защита металлов
Если рассмотреть статистику, то можно отметить, что практически 30% от общей массы эксплуатируемого металла подвергается такому разрушительному процессу, как коррозия металла. И десятая часть уходит в отходы, остальная правда переплавляется.
Чем же отвечает научно-технический прогресс коррозии металлов? Только созданием хороших коррозионно-стойких материалов и технологий, которые могут создать условия, при которых коррозия невозможна.
Защита металла от коррозии включает в себя несколько способов, которые доказали, что с этим процессом можно эффективно бороться.
Многие методы борьбы с коррозией металлов известны давно и прекрасно используются в настоящее время. Первый способ – это изоляция от агрессивной среды.
Здесь необходимо отметить:
- Всевозможные полимерные пленки;
- Лаки;
- Краски;
- Олифы.
Так и металлы, которыми покрывают металл в виде слоя, не разрушающегося под воздействием агрессивных сред.
Разрушительное действие коррозии
Покраска металлических поверхностей против их разрушения используется давно и считается первым способом защиты металлов от коррозии.
Проводить данную операцию несложно. Кстати, эта защита металлов считается одной из эффективных. Но здесь необходимо соблюдать некоторые правила.
Первый этап – это очистка металлических поверхностей от загрязнений. Он считается как подготовительным этапом, так и самым главным, потому что нанесение краски на поверхность, которую не очистили, приведет к нулевому результату.Особое внимание при проведении очистки необходимо уделять удалению грязи, ржавчины и жирных пятен.
Второй этап – грунтовка поверхности. Этот процесс необходим для одной лишь цели – это сцепление краски и поверхности металла. Если данную процедуру не проводить, то краска долго держаться не будет и через непродолжительное время облупится и сойдет с поверхности.
Третий этап – это сам процесс нанесения антикоррозионной краски. В данной ситуации используется несколько способов нанесения краски.
Традиционным является использование молярных инструментов, таких как валик и кисти, этот способ называется ручным. И еще один способ – с помощью краскопульта, который считается более экономичным.
Современный рынок строительных материалов в настоящее время предлагает огромный выбор всевозможной лакокрасочной продукции, которая прекрасно справляется с коррозией.
Сейчас можно также сказать о том, что компании-производители антикоррозионной краски стали выпускать особые краски, которые прекрасно справляются с очень агрессивными средами.Такая защита может противостоять даже морской воде.
А вот использование различных пленок на основе полимеров при защите металлов от коррозии в настоящее время стало принимать массовый характер. И это понятно, ведь данный вид покрытий имеет ряд преимуществ, к которым относятся:
- Высокий уровень водостойкости;
- Высокий показатель противостояния химическому воздействию.
Но необходимо отметить, что данный метод является более дорогим по сравнению с покраской.
Влажный климат для коррозии — идеальная среда
Если металлические конструкции или изделия расположены под землей, к примеру, трубопровод, то иногда используют для защиты такие материалы, как битум, асфальт, различные полимерные ленты.
Конечно, сравнивать вышеуказанные способы с покрытием поверхности металлов другими металлами или другими материалами нельзя, потому что последний считается самым эффективным. К примеру, процесс лужения, где на поверхность металла наносится слой олова.
Или процесс гуммирования, где металл обрабатывается каучуком. Правда, данные процессы достаточно дороги, но защита при этом самая эффективная.Второй способ, где коррозия металлов удерживается под воздействием изменения электрической направленности.
То есть, если металлическая конструкция установлена в грунт, то рядом устанавливают специальный стержень из более активного металла (алюминий, цинк), который подсоединен к источнику электрического тока.
Основная конструкция и стержень также соединены между собой проводником. Полярность конструкции меняется, и она из анода переходит в разряд катода. То есть заряжается отрицательными зарядами.
Стержень берет на себя все положительно заряженные ионы и разрушается, то есть происходит его коррозия.
Третий способ. Коррозия металла, как процесс разрушения, может быть остановлен, а точнее сказать, замедлен путем добавления в агрессивные среды органических или неорганических ингибиторов. Обычно данный способ используется при очистке:
- Паровых котлов;
- Емкостей под соляную кислоту;
- Различных деталей с окалиной.
Использование ингибиторов стало возможным только по одной причине, они при взаимодействии с металлом создают на его поверхности пленку, которая состоит из трудно растворимых соединений.
Тем самым создается покрытие, которое отличается высокой прочностью. Кстати, толщина ингибиторного покрытия намного меньше, чем толщина любого искусственного антикоррозионного покрытия.Такая защита часто используется в котельных, где внутри котлов всегда агрессивная среда.
В настоящее время еще в стадии проектирования строительные компании стараются собрать всю информацию, касающуюся характера агрессивных воздействий и условия эксплуатации металлических конструкций.
От собранной информации будут зависеть проектные решения, то есть сегодня во главу угла ставятся в основном показатели, которые будут влиять на срок эксплуатации здания или сооружения.Лабораторные исследования и современные разработки сегодня принимаются во внимание в первую очередь при проведении антикоррозионных работ. А использование новейших материалов является залогом успешной защиты металлических конструкций от коррозии.
Иногда даже маленькая деталь может стать причиной нестабильности всей конструкции
Особенно большое значение придается натурным обследованиям уже существующих зданий и сооружений.
Именно на их примере можно с большой вероятностью определить качество и долговечность антикоррозийных материалов. Кстати, в этой области накоплен достаточно большой опыт.
Сегодня говорить о том, что коррозия металла как процесс его разрушения практически побежден, преждевременно. И проблем здесь хватает. Но ученые прилагают все усилия, чтобы коррозия металла как можно меньше доставляла неудобств в процессе эксплуатации металлических конструкций.
Все больше появляется методов борьбы с этим процессом, все больше появляется материалов, которые гарантируют эффективную защиту.
На исследования тратятся большие финансовые средства, поэтому коррозия металла должна отступить в будущем, а точнее сказать, сдать свои позиции. Коррозия металлов и меры борьбы с ней – это одна из главных задач, которую ставят перед собой строители, начиная поднимать новый объект.
Коррозия металлов
Коррозия – разрушение поверхности сталей и сплавов под воздействием различных физико-химических факторов – наносит огромный ущерб деталям и металлоконструкциям. Ежегодно этот невидимый враг «съедает» около 13 млн. т металла.
Для сравнения – металлургическая промышленность стран Евросоюза в прошлом, 2014 году произвела всего на 0,5 млн. тонн больше. И это только – прямые потери.
А длительная эксплуатация стальных изделий без их эффективной защиты от коррозии вообще невозможна.
Что такое коррозия и её разновидности
Основной причиной интенсивного окисления поверхности металлов (что и является основной причиной коррозии) являются:
- Повышенная влажность окружающей среды.
- Наличие блуждающих токов.
- Неблагоприятный состав атмосферы.
Соответственно этому различают химическую, трибохимическую и электрохимическую природу коррозии. Именно они в совокупности своего влияния и разрушают основную массу металла.
Химическая коррозия
Такой вид коррозии обусловлен активным окислением поверхности металла во влажной среде. Безусловным лидером тут является сталь (исключая нержавеющую).
Железо, являясь основным компонентом стали, при взаимодействии с кислородом образует три вида окислов: FeO, Fe2O3 и Fe3O4.
Основная неприятность заключается в том, что определённому диапазону внешних температур соответствует свой окисел, поэтому практическая защита стали от коррозии наблюдается только при температурах выше 10000С, когда толстая плёнка высокотемпературного оксида FeO сама начинает предохранять металл от последующего образования ржавчины. Это процесс называется воронением, и активно применяется в технике для защиты поверхности стальных изделий. Но это – частный случай, и таким способом активно защищать металл от коррозии в большинстве случаев невозможно.
Химическая коррозия активизируется при повышенных температурах. Склонность металлов к химическому окислению определяется значением их кислородного потенциала – способности к участию в окислительно-восстановительных реакциях. Сталь – ещё не самый худший вариант: интенсивнее её окисляются, в частности, свинец, кобальт, никель.
Электрохимическая коррозия
Эта разновидность коррозии более коварна: разрушение металла в данном случае происходит при совокупном влиянии воды и почвы на стальную поверхность (например, подземных трубопроводов).
Влажный грунт, являясь слабощёлочной средой, способствует образованию и перемещению в почве блуждающих электрических токов. Они являются следствием ионизации частиц металла в кислородсодержащей среде, и инициирует перенос катионов металла с поверхности вовне.
Борьба с такой коррозией усложняется труднодоступностью диагностирования состояния грунта в месте прокладки стальной коммуникации.
Электрохимическая коррозия возникает при окислении контактных устройств линий электропередач при увеличении зазоров между элементами электрической цепи. Помимо их разрушения, в данном случае резко увеличивается энергопотребление устройств.Трибохимическая коррозия
Данному виду подвержены металлообрабатывающие инструменты, которые работают в режимах повышенных температур и давлений. Антикоррозионное покрытие резцов, пуансонов, фильер и пр. невозможно, поскольку от детали требуется высокая поверхностная твёрдость.
Между тем, при скоростном резании, холодном прессовании и других энергоёмких процессах обработки металлов начинают происходить механохимические реакции, интенсивность которых возрастает с увеличением температуры на контактной поверхности «инструмент-заготовка».
Образующаяся при этом окись железа Fe2O3 отличается повышенной твёрдостью, и поэтому начинает интенсивно разрушать поверхность инструмента.
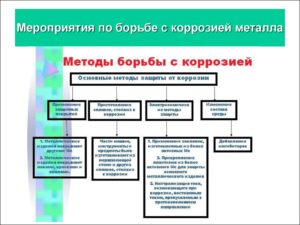
Методы борьбы с коррозией
Выбор подходящего способа защиты поверхности от образования ржавчины определяется условиями, в которых работает данная деталь или конструкция. Наиболее эффективны следующие методы:
- Нанесение поверхностных атмосферостойких покрытий;
- Поверхностная металлизация;
- Легирование металла элементами, обладающими большей стойкостью к участию в окислительно-восстановительных реакциях;
- Изменение химического состава окружающей среды.
Механические поверхностные покрытия
Поверхностная защита металла может быть выполнена его окрашиванием либо нанесением поверхностных плёнок, по своему составу нейтральных к воздействию кислорода. В быту, а также при обработке сравнительно больших площадей (главным образом, подземных трубопроводов) применяется окраска.
Среди наиболее стойких красок – эмали и краски, содержащие алюминий.
В первом случае эффект достигается перекрытием доступа кислороду к стальной поверхности, а во втором – нанесением алюминия на поверхность, который, являясь химически инертным металлом, предохраняет сталь от коррозионного разрушения.
Положительными особенностями данного способа защиты являются лёгкость его реализации и сравнительно небольшие финансовые затраты, поскольку процесс достаточно просто механизируется. Вместе с тем долговечность такого способа защиты невелика, поскольку, не обладая большой степенью сродства с основным металлом, такие покрытия через некоторое время начинают механически разрушаться.
Химические поверхностные покрытия
Коррозионная защита в данном случае происходит вследствие образования на поверхности обрабатываемого металла химической плёнки, состоящей из компонентов, стойких к воздействию кислорода, давлений, температур и влажности. Например, углеродистые стали обрабатывают фосфатированием.
Процесс может выполняться как в холодном, так и в горячем состоянии, и заключается в формировании на поверхности металла слоя из фосфатных солей марганца и цинка. Аналогом фосфатированию выступает оксалатирование – процесс обработки металла солями щавелевой кислоты.
Применением именно таких технологий повышают стойкость металлов от трибохимической коррозии.
Недостатком данных методов является трудоёмкость и сложность их применения, требующая наличия специального оборудования. Кроме того, конечная поверхность изменяет свой цвет, что не всегда приемлемо по эстетическим соображениям.
Легирование и металлизация
В отличие от предыдущих способов, здесь конечным результатом является образование слоя металла, химически инертного к воздействию кислорода. К числу таких металлов относятся те, которые на линии кислородной активности находятся возможно дальше от водорода. По мере возрастания эффективности этот ряд выглядит так: хром→медь→цинк→серебро→алюминий→платина.
Различие в технологиях получения таких антикоррозионных слоёв состоит в способе их нанесения.
При металлизации на поверхность направляется ионизированный дуговой поток мелкодисперсного напыляемого металла, а легирование реализуется в процессе выплавки металла, как следствие протекания металлургических реакций между основным металлом и вводимыми легирующими добавками.
Изменение состава окружающей среды
В некоторых случаях существенного снижения коррозии удаётся добиться изменением состава атмосферы, в которой работает защищаемая металлоконструкция. Это может быть вакуумирование (для сравнительно небольших объектов), или работа в среде инертных газов (аргон, неон, ксенон).
Данный метод весьма эффективен, однако требует дополнительного оборудования — защитных камер, костюмов для обслуживающего персонала и т.д.
Используется он главным образом, в научно-исследовательских лабораториях и опытных производствах, где специально поддерживается необходимый микроклимат.
Кто нам мешает, тот нам поможет
В завершение укажем и на довольно необычный способ коррозионной защиты: с помощью самих окислов железа, точнее, одного из них — закиси-окиси Fe3O4. Данное вещество образуется при температурах 250…5000С и по своим механическим свойствам представляет собой высоковязкую технологическую смазку.
Присутствуя на поверхности заготовки, Fe3O4 перекрывает доступ кислороду воздуха при полугорячей деформации металлов и сплавов, и тем самым блокирует процесс зарождения трибохимической коррозии. Это явление используется при скоростной высадке труднодеформируемых металлов и сплавов.
Эффективность данного способа обусловлена тем, что при каждом технологическом цикле контактные поверхности обновляются, а потому стабильность процесса регулируется автоматически.
Оставляете заявку на сайте или по телефону
Оцениваем запрос и тех. документацию
Осматриваем объект
Подготавливаем КП
Сдаем работу заказчику
Выполняем работы
Разрабатываем рабочую документацию
Заключаем договор
Наши преимущества
Подготовленный персонал, находящийся постоянно в штате
Наличие богатого технического оснащения
Гарантийное и послегарантийное обслуживание
Самый большой спектр услуг в России
Большой опыт работы на разнотипных объектах
Эффективные методы борьбы с коррозией кузова авто. Как убрать коррозию своими руками
Борьба с коррозией авто зачастую доставляет массу проблем его владельцу. Для этого используют три основных метода — пассивный, активный и электрохимический, но каждый из них имеет свои преимущества и недостатки.
Чаще всего коррозию удаляют с помощью специальных средств. А в целях профилактики на днище, пороги корпуса и другие скрытые места наклеивают защитную пленку или обрабатывают мастикой.
Также существуют другие профилактические средства, о которых мы поговорим с вами далее.
Причины возникновения коррозии
Для начала разберемся, почему же возникают коррозионные процессы. Дело в том, что коррозия металлических поверхностей бывает четырех типов — электрохимическая, химическая, водородная и кислородная. В контексте ржавления автомобильного корпуса имеют место лишь первые два типа.
Электрохимическая коррозия возникает по причине того, что два материала с разными восстановительными свойствами взаимодействуют через электролит (любая недистиллированная вода является таковым).
Поскольку железо обладает низкими восстановительными свойствами, то оно значительно подвержено ржавлению. Химическая коррозия происходит из-за взаимодействия поверхности металла и коррозионно-активной среды. В роли последней может выступать кислород при высоких температурах.Понимание сути возникающих процессов дает нам почву для поиска методов борьбы с коррозией.
Виды борьбы с коррозией
Существует два основных способа защиты кузова машины от коррозии. Первый — это барьерная защита. Она не допускает физическое взаимодействие поверхности уязвимых металлов с внешней средой. Это выражается в использовании лакокрасочного покрытия и различных механических средств и защит.