Производство водорода электролизом
Производство водорода электролизом — Справочник металлиста
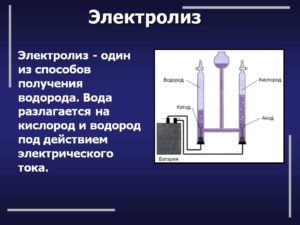
Электролиз широко используется в производственной сфере, например, для получения алюминия (аппараты с обожженными анодами РА-300, РА-400, РА-550 и т.д.) или хлора (промышленные установки Asahi Kasei).
В быту этот электрохимический процесс применялся значительно реже, в качестве примера можно привести электролизер для бассейна Intellichlor или плазменный сварочный аппарат Star 7000.
Увеличение стоимости топлива, тарифов на газ и отопление в корне поменяли ситуацию, сделав популярной идею электролиза воды в домашних условиях.
Рассмотрим, что представляют собой устройства для расщепления воды (электролизеры), и какова их конструкция, а также, как сделать простой аппарат своими руками.
Что такое электролизер, его характеристики и применение
Так называют устройство для одноименного электрохимического процесса, которому требуется внешний источник питания. Конструктивно это аппарат представляет собой заполненную электролитом ванну, в которую помещены два или более электродов.
Основная характеристика подобных устройств – производительность, часто это параметр указывается в наименовании модели, например, в стационарных электролизных установках СЭУ-10, СЭУ-20, СЭУ-40, МБЭ-125 (мембранные блочные электролизеры) и т.д. В данных случаях цифры указывают на выработку водорода (м3/ч).
Промышленная стационарная электролизная установка, вырабатывающая 40 м3 водорода в час (СЭУ-40)
Что касается остальных характеристик, то они зависят от конкретного типа устройства и сферы применения, например, когда осуществляется электролиз воды, на КПД установки влияют следующие параметры:
- Уровень напряжения (минимального электродного потенциала), оно должно быть от 1,8 до 2 вольт, меньшее значение «не запустит» процесс, а большее приводит к чрезмерному расходу энергии, идущей на нагрев электролита. Если в качестве источника используется блок питания, например, на 14 вольт имеет смысл разделить емкость ванны пластинами на 7 ячеек, в соответствии с рисунком 2.Рис 2. Расположение пластин в ванне электролизера
Таким образом, подавая на выходы 14 вольт, мы получим 2 вольта на каждой ячейке, при этом на пластинах с каждой стороны будут разные потенциалы. Электролизеры, где используется подобная система подключения пластин, называются сухими.
- Расстояние между пластинами (между катодным и анодным пространством), чем оно меньше, тем меньше будет сопротивление и, следовательно, больший ток пройдет через раствор электролита, что приведет к увеличению выработки газа.
- Размеры пластины (имеется в виду площадь электродов), прямо пропорциональны току, идущему через электролит, а значит, также оказывают влияние на производительность.
- Концентрация электролита и его тепловой баланс.
- Характеристики материала, используемого для изготовления электродов (золото – идеальный материал, но слишком дорогой, поэтому в самодельных схемах используется нержавейка).
- Применение катализаторов процесса и т.д.
Как уже упоминалось выше, установки данного типа могут использоваться как генератор водорода, для получения хлора, алюминия или других веществ. Они также применяются в качестве устройств, при помощи которых осуществляется очистка и обеззараживание воды (УПЭВ, VGE), а также проводится сравнительный анализ ее качества (Tesp 001).
А) Установка прямого электролиза воды (УПЭВ); Б) анализатор качества воды Tesp 001
Нас, прежде всего, интересуют устройства, производящие газ Брауна (водород с кислородом), поскольку именно эта смесь имеет все перспективы для использования в качестве альтернативного энергоносителя или добавок к топливу. Их мы рассмотрим чуть позже, а пока перейдем к конструкции и принципу работы простейшего электролизера, расщепляющего воду на водород и кислород.
Устройство и подробный принцип работы
Аппараты для производства гремучего газа, в целях безопасности, не предполагают его накопление, то есть газовая смесь сжигается сразу после получения.
Это несколько упрощает конструкцию.
В предыдущем разделе мы рассмотрели основные критерии, влияющие на производительность аппарата и накладывающие определенные требования к исполнению.
Принцип работы устройства демонстрирует рисунок 4, источник постоянного напряжения подключен к погруженным в раствор электролита электродам. В результате через него начинает проходить ток, напряжение которого выше точки разложения молекул воды.
Рисунок 4. Конструкция простого электролизера
В результате этого электрохимического процесса катод выделяет водород, а анод – кислород, в соотношении 2 к 1.
Виды электролизеров
Кратко ознакомимся с конструктивными особенностями основных видов устройств для расщепления воды.
Сухие
Конструкция прибора данного типа была показана на рисунке 2, ее особенность заключается в том, что манипулируя количеством ячеек, можно запитать устройство от источника с напряжением, существенно превышающим минимальный электродный потенциал.
Проточные
С упрощенным устройством приборов этого вида можно ознакомиться на рисунке 5. Как видим, конструкция включает в себя ванну с электродами «A», полностью залитую раствором и бак «D».
Рис 5. Конструкция проточного электролизера
Принцип работы устройства следующий:
- входе электрохимического процесса газ вместе с электролитом выдавливается в емкость «D» через трубу «В»;
- в баке «D» происходит отделение от электролитного раствора газа, который выводится через выходной клапан «С»;
- электролит возвращается в гидролизную ванну через трубу «Е».
Мембранные
Основная особенность устройств этого типа – использование твердого электролита (мембраны) на полимерной основе. С конструкцией приборов этого вида можно ознакомиться на рисунке 6.
Рис 6. Электролизер мембранного типа
Основная особенность таких устройств заключается в двойном назначении мембраны, она не только переносит протоны и ионы, а и на физическом уровне разделяет как электроды, так и продукты электрохимического процесса.
Диафрагменные
В тех случаях, когда не допустима диффузия продуктов электролиза между электродными камерами, используют пористую диафрагму (что и дало название таким приборам).
Материалом для нее может служить керамика, асбест или стекло. В некоторых случаях для создания такой диафрагмы можно использовать полимерные волокна или стеклянную вату.
На рисунке 7 показан простейший вариант диафрагменного прибора для электрохимических процессов.
Конструкция диафрагменного электролизера
Пояснение:
- Выход для кислорода.
- U-образная колба.
- Выход для водорода.
- Анод.
- Катод.
- Диафрагма.
Щелочные
Электрохимический процесс невозможен в дистиллированной воде, в качестве катализатора применяется концентрированный раствор щелочи (использование соли нежелательно, так как при этом выделяется хлор). Исходя из этого, щелочными можно назвать большую часть электрохимических устройств для расщепления воды.
На тематических форумах советуют использовать гидроксид натрия (NaOH), который, в отличие от пищевой соды (NaHCO3), не разъедает электрод. Заметим, что у последней имеются два весомых преимущества:
- Можно использовать железные электроды.
- Не выделяются вредные вещества.
Но, один существенный недостаток сводит на нет все преимущества пищевой соды, как катализатора. Ее концентрация в воде не более 80 грамм на литр.
Это снижает морозостойкость электролита и его проводимость тока.
Если с первым еще можно смириться в теплое время года, то второе требует увеличения площади пластин электродов, что в свою очередь, увеличивает размер конструкции.
Электролизер для получения водорода: чертежи, схема
Рассмотрим, как можно сделать мощную газовую горелку, работающую от смеси водорода с кислородом. Схему такого устройства можно посмотреть на рисунке 8.
Рис. 8. Устройство водородной горелки
Пояснение:
- Сопло горелки.
- Резиновые трубки.
- Второй водяной затвор.
- Первый водяной затвор.
- Анод.
- Катод.
- Электроды.
- Ванна электролизера.
На рисунке 9 представлена принципиальная схема блока питания для электролизера нашей горелки.
Рис. 9. Блок питания электролизной горелки
На мощный выпрямитель нам понадобятся следующие детали:
- Транзисторы: VT1 – МП26Б; VT2 – П308.
- Тиристоры: VS1 – КУ202Н.
- Диоды: VD1-VD4 – Д232; VD5 – Д226Б; VD6, VD7 – Д814Б.
- Конденсаторы: 0,5 мкФ.
- Переменные резисторы: R3 -22 кОм.
- Резисторы: R1 – 30 кОм; R2 – 15 кОм; R4 – 800 Ом; R5 – 2,7 кОм; R6 – 3 кОм; R7 – 10 кОм.
- PA1 – амперметр со шкалой измерения не менее 20 А.
Краткая инструкция по деталям к электролизеру.
Ванну можно сделать из старого аккумулятора. Пластины следует нарезать 150х150 мм из кровельного железа (толщина листа 0,5 мм). Для работы с вышеописанным блоком питания потребуется собрать электролизер на 81 ячейку. Чертеж, по которому выполняется монтаж, приведен на рисунке 10.
Рис. 10. Чертеж электролизера для водородной горелки
Заметим, что обслуживание такого устройства и управление им не вызывает трудностей.
Электролизер для автомобиля своими руками
В интернете можно найти много схем HHO систем, которые, если верить авторам, позволяют экономить от 30% до 50% топлива. Такие заявления слишком оптимистичны и, как правило, не подтверждаются никакими доказательствами. Упрощенная схема такой системы продемонстрирована на 11 рисунке.
Водород при сотнях градусов — реальность или фантастика?
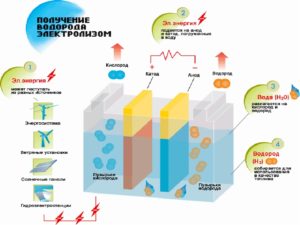
Высокотемпературный электролиз (также известен как электролиз водяного пара) – технология производства водорода и/или угарного газа из воды и/или углекислого газа с побочным продуктом в виде кислорода.
КПД
С экономической точки зрения высокотемпературный электролиз гораздо эффективнее, чем традиционный электролиз при комнатной температуре, так как некоторая часть энергии подается в виде тепла, более дешевого по сравнению с электричеством, а также потому, что реакция электролиза гораздо продуктивнее протекает при высоких температурах. Фактически при 2500C электрический ток не требуется, потому что вода распадается на водород и кислород путем термолиза. Подобные температуры являются практически нецелесообразными; предлагаемые ВТЭ работают в диапазоне 100-850C.
Увеличение КПД высокотемпературного электролиза лучше всего произойдет за счет оценки количества используемого электричества, поступающего из теплового двигателя, а затем – учета количества тепловой энергии, нужной для производства одного килограмма водорода (141,86 МДж), как во время самого процесса электролиза, так и во время производства электричества. При 100C требуется 350 МДж тепловой энергии (КПД – 41 %). При 850C требуется 225 МДж тепловой энергии (КПД – 64 %).
Материалы
Крайне важен подбор материалов для электродов и электролита в твердом оксидном электролизном элементе. Один из вариантов – диоксид циркония, стабилизированный оксидом иттрия в качестве электролита, никель-керметовые электроды для водяного пара или водорода, и смесь оксидов лантана, стронция и кобальта для кислородных электродов.
Экономический потенциал
Даже с использованием этой технологии электролиз является откровенно невыгодным способом хранения энергии. Серьезные потери энергии при преобразовании происходят как во время процесса электролиза, так и во время преобразования полученного водорода обратно в энергию.
При текущих ценах на углеводороды ВТЭ не может конкурировать с пиролизом углеводородов, как экономическим источником водорода.
ВТЭ представляет собой интерес, как гораздо более эффективный способ производства водорода, при условии использования безуглеродного топлива и стандартных схем хранения энергии.
Это может стать экономически выгодным, если дешевые альтернативные источники тепловой энергии (сконцентрированная солнечная, ядерная, геотермальная) можно будет использовать в связке с альтернативными источниками электроэнергии (солнечная, ветряная, водная, ядерная).
Возможными источниками дешевой высокотемпературной тепловой энергии будут исключительно нехимические виды, в том числе – ядерные реакторы, коллекторы, собирающие солнечное тепло, и геотермальные источники.
В лабораторных условиях высокотемпературный электролиз показал затраты в 108 кДж для производства одного грамма водорода. В коммерческих условиях он себя не проявлял.
К 2030 году ожидается постройка первых коммерческих реакторов четвертого поколения.
Рынок производства водорода
При обеспечении дешевыми источниками тепла высокой температуры возможны и другие способы производства водорода. В частности, стоит обратить внимание на термохимический серно-йодный цикл.
Термохимическое производство может быть эффективнее, чем ВТЭ из-за отсутствия потребности в тепловом двигателе.
Однако промышленное термохимическое производство потребует новых передовых материалов, которые смогут выдерживать высокие температуру, давление и коррозию.
Рынок для водорода – велик (50 миллионов метрических тонн/год в 2004 году, стоимость – около 135 миллиардов долларов/год) и растет примерно на 10 % в год. Этот рынок связан с пиролизом углеводородов для получения водорода, что приводит к выбросам углекислого газа.
Два главных потребителя – нефтеперерабатывающие заводы и производители удобрений (каждый из них получит примерно половину всего производства).
Автомобили на водороде должны распространиться повсеместно, их потребление вырастет, что поможет увеличить потребность в водороде при приходе водородной энергетики.
Электролиз и термодинамика
Во время электролиза объем электроэнергии, который необходимо добавить, равен сумме изменения энергии Гиббса в реакции и потерь системы.
Теоретически потери могут быть сколь угодно близки к нулю, поэтому максимальный термодинамический КПД любого электрохимического процесса равен 100%.
На практике КПД равен полученной работе электричества, разделенному на изменение энергии Гиббса во время реакции.
В большинстве случаев, как и при обычном электролизе воды, потребляемая мощность больше, чем изменение теплосодержания в реакции, поэтому некоторое количество энергии высвобождается в виде сбросного тепла. В случае электролиза водяного пара на водород и кислород при высокой температуре верно обратное.Тепло поглощается из окружающей среды, и удельная теплота сгорания производимого водорода выше потребляемой мощности. В этом случае отношение КПД к потребляемой мощности, можно сказать, превышает 100%. Максимально возможный в теории КПД топливного элемента противоположен КПД при электролизе.
Из этого следует невозможность создания вечного двигателя путем сочетания этих двух процессов.
Эксперимент «MARS ISRU»
Высокотемпературный электролиз с твердыми оксидными электролизными элементами также предлагался для производства кислорода на Марсе из атмосферного углекислого газа с использованием циркониевых электролизных устройств.