Защита металла в земле от коррозии
Защита металла в земле от коррозии — Справочник металлиста

Развитие сталелитейной промышленности неразрывно связано с поиском способов и средств, предотвращающих разрушение металлических изделий.
Защита от коррозии, разработка новых методик – это непрерывный процесс в технологической цепочке производства металла, изделий из него.
Железосодержащие изделия приходят в негодность под воздействием различных физико-химических внешних факторов среды. Эти последствия мы видим в виде гидратированных остатков железа, то есть ржавчины.
Виды коррозии
Способы защиты металлов от коррозии подбираются в зависимости от условий эксплуатации изделий. Поэтому выделяется:
- Коррозия, связанная с атмосферными явлениями. Это разрушительный процесс кислородной или водородной деполяризации металла. Что приводит к разрушению кристаллической молекулярной решетки под воздействием влажной среды воздуха и других агрессивных факторов и примесей (температура, наличие химических примесей и т.д.).
- Коррозия в воде, в первую очередь морской. В ней процесс проходит быстрее из-за содержания солей и микроорганизмов.
- Процессы разрушения, которые происходят в грунте. Почвенная коррозия – довольно сложная форма повреждения металла. Многое зависит от состава почвы, влажности, прогрева и других факторов. К тому же изделия, к примеру, трубопроводы, зарыты глубоко в земле, что затрудняет диагностику. А коррозия поражает часто отдельные участи точечно или в виде язвенных жил.
Виды защиты от коррозии подбираются индивидуально, отталкиваются от того, в какой среде будет находиться защищаемое металлическое изделие.
Характерные типы поражения ржавчиной
Способы защиты стали и сплавов зависят не только от вида коррозии, но и от типа разрушения:
- Ржавчина покрывает поверхность изделия сплошным слоем или отдельными участками.
- Выступает в виде пятен и точечно проникает вглубь детали.
- Разрушает металлическую молекулярную решетку в виде глубокой трещины.
- В стальном изделии, состоящем из сплавов, происходит разрушение одного из металлов.
- Более глубокое обширное ржавление, когда не только постепенно нарушается поверхность, но и происходит проникновение в глубокие слои конструкции.
Типы поражения могут быть комбинированные. Иногда их трудно определить сразу, особенно когда происходит точечное разрушение стали. Методы защиты от коррозии включают в себя специальную диагностику для определения степени повреждений.
Выделяют химическую коррозию без возникновения электрических токов. При соприкосновении с нефтепродуктами, спиртовыми растворами и другими агрессивными ингредиентами происходит химическая реакция, сопровождаемая газовыми выделениями и высокой температурой.
Электрохимическая коррозия — это когда металлическая поверхность контактирует с электролитом, в частности с водой из окружающей среды. В этом случае происходит диффузия металлов. Под воздействием электролита возникает электрический ток, происходит замещение и движение электронов металлов, которые входят в сплав. Структура разрушается, образуется ржавчина.Выплавка стали и ее коррозионная защита – это две стороны одной медали. Коррозия наносит огромный вред промышленным и хозяйственным постройкам. В случаях с масштабными техническими сооружениями, к примеру, мостами, опорами электропередач, заградительными сооружениями, может спровоцировать и техногенные катастрофы.
Коррозия металла и способы защиты от нее
Как защитить металл? Коррозия металлов и способы защиты от нее существует много. Чтобы предохранить металл от ржавчины, используют промышленные методы. В бытовых условиях применяются различные силиконовые эмали, лаки, краски, полимерные материалы.
Промышленные
Защиту железа от коррозии можно подразделить на несколько основных направлений. Способы защиты от коррозии:
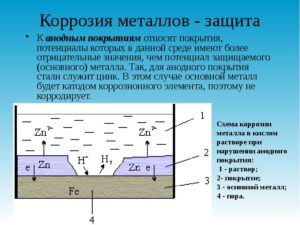
- Пассивация. При получении стали добавляют другие металлы (хром, никель, молибден, ниобий и другие). Они отличаются повышенными качественными характеристиками, тугоплавкостью, устойчивостью к агрессивным средам и т.д. В результате образуется оксидная пленка. Такие виды стали называют легированными.
- Покрытие поверхности другими металлами. Методы защиты металлов от коррозии используются разные: гальваника, погружение в расплавленный состав, нанесение на поверхность с помощью специального оборудования. В результате образуется металлическая защитная пленка. Чаще всего применяются для этих целей хром, никель, кобальт, алюминий и другие. Используют и сплавы (бронзу, латунь).
- Использование металлических анодов, протекторов, чаще из магниевых сплавов, цинка или алюминия. В результате соприкосновением с электролитом (водой), начинается электрохимическая реакция. Протектор разрушается и образует на поверхности стали защитную пленку. Эта методика хорошо зарекомендовала себя для подводных деталей судов и буровых установок в море.
- Ингибиторы кислотного травления. Использование веществ, которые снижают уровень воздействия окружающей среды на металл. Они применяются для консервации, хранения изделий. А также в нефтеперерабатывающей промышленности.
- Коррозия и защита металлов, биметаллы (плакирование). Это покрытие стали слоем другого металла или композитным составом. Под воздействием давления и высоких температур происходит диффузия и склеивание поверхностей. К примеру, всем известные радиаторы отопления из биметалла.
Коррозия металла и способы защиты от нее, применяемые в промышленном производстве, достаточно разнообразны, это химическая защита, покрытие стеклоэмалью, эмалированные изделия. Сталь закаляют при высоких, свыше 1000 градусов, температурах.
На видео: цинкование металла как защита против коррозии.
Бытовые
Защита металлов от коррозии в домашних условиях – это, в первую очередь, химия для производства лакокрасочных материалов. Защитные свойства составов достигаются путем комбинирования различных компонентов: силиконовых смол, полимерных материалов, ингибиторов, металлической пудры и стружки.
Предохраняя поверхность от ржавчины, необходимо перед покраской, особенно старых конструкций, использовать специальные грунтовки или преобразователь ржавчины.
Какие виды преобразователей бывают:
- Грунтующие средства — обеспечивают адгезию, схватываемость с металлом, выравнивают поверхность перед окрашиванием. Большая часть из них содержит ингибиторы, которые значительно замедляют процесс коррозии. Предварительное нанесение грунтующего слоя позволяет значительно сэкономить краску.
- Химические соединения — превращают окись железа в другие соединения. Они не подвержены ржавлению. Их называют стабилизаторами.
- Составы, которые преобразуют ржавчину в соли.
- Смолы и масла, связывающие и уплотняющие ржавчину, таким образом нейтрализуя ее.
В состав этих средств входят компоненты, которые максимально замедляют процесс образование ржавчины. Преобразователи включены в линейку товаров производителей, выпускающих краски по металлу. По своей консистенции они бывают разные.
Лучше выбирать грунтовку и краску одной фирмы, чтобы они подходили по химическому составу. Предварительно необходимо определиться, какие способы вы выберете для нанесения состава.
Защитные краски по металлу
Краски по металлу подразделяются на термоустойчивые, которые можно эксплуатировать при высоких температурах, и для обычного температурного режима до восьмидесяти градусов.
Используют такие основные виды красок по металлу: алкидные, акриловые, эпоксидные краски. Существуют специальные антикоррозийные краски. Они двух- или трехкомпонентные.
Их смешивают непосредственно перед употреблением.
Как защитить металл от коррозии в домашних условиях
Минувший век характеризуется возникновением огромного количества принципиально новых материалов, нашедших широкое применение в разнообразнейших отраслях человеческой жизнедеятельности, включая и строительную.
Собственно говоря, в материаловедении произошла подлинная революция, причем значительное внимание было уделено вопросам предотвращения коррозии металлов и разработке материалов, необходимых для достижения этой цели.
Так, например, появились различные композитные панели, гальванические покрытия, облицовочные материалы из строительной керамики (керамогранит, облицовочный кирпич и т. д.), прочие современные строительные материалы, не нуждающиеся в защите путем дополнительной обработки.
Применение в строительстве металлических изделий, как и прежде, остается востребованным чрезвычайно широко. Перила, декоративные решетки и ограждения даже сегодня чаще всего изготавливают из металлов, которые подвержены коррозии.
Так, отделка фасадов, которую в наше время осуществляют посредством использования тех или иных материалов, устойчивых к воздействию атмосферной влаги, все же не обходится без применения крепежа, узлов ввода-вывода коммуникаций, иных скрытых элементов.
Данные компоненты наиболее часто выполняются из металла, а потому жизненно нуждаются в антикоррозионной защите.
Хорошо известно, что основной причиной коррозии является вода, которая неминуемо попадает на металлические поверхности даже в помещениях. А потому наиболее эффективным и, пожалуй, единственным способом защиты металлов, подверженных коррозии, является нанесение изолирующих составов и химических покрытий.
К традиционным способам предохранения металлических изделий от коррозии относится механическая зачистка старой ржавчины, а также нанесение преобразователей ржавчины, позволяющих удалить ее остатки, после чего поверхность металла покрывается грунтом и лакокрасочным защитным слоем.
Некоторые из производителей лакокрасочных материалов рекомендуют осуществить завершение этого процесса путем нанесения поверх слоя краски специального защитного состава.
При этом основное внимание необходимо обратить на то, чтобы грунтовки, краски и лаки были качественными.
На упаковках с грунтами указываются виды специальных добавок, улучшающих свойства состава: изолирующих, фосфатирующих, пассивирующих и протектирующих.Как видим, окраска металлических поверхностей «по старинке» — процесс достаточно сложный и трудоемкий, отнимающий много сил и времени.
Ныне компании-производители рекомендуют разработанные ими антикоррозионные составы, отличающиеся большей универсальностью, применение которых позволяет одновременно решать не какую-либо одну, а сразу несколько задач. Наиболее популярными среди потребителей являются так называемые средства «два в одном» и «три в одном».
Краска «два в одном» сочетает в себе находящиеся в одной емкости грунтующий и окрашивающий составы, при помощи которых возможно выполнение как грунтования, так и окончательной окраски металлических поверхностей.
Нередко производителями подобных красок рекомендуется использование составов типа «два в одном» по предварительно огрунтованным поверхностям, работающим в агрессивных средах, к примеру для кровли.
Композиции «три в одном», кроме грунта и краски, включают в свой состав также и преобразователь ржавчины. Их целесообразно использовать при окрашивании сильно заржавевших поверхностей, при этом необходимо удалить лишь верхний рыхлый слой ржавчины. На упаковках подобных составов обычно можно видеть надпись — непосредственно на ржавчину.
Может ли вода защитить металл от коррозии?
Казалось бы как вообще такое возможно? Этого не может быть, потому что этого быть не может никогда! Однако прогресс не стоит на месте. Он стремительно движется вперед во всех отраслях, в т. ч. и в сфере разработок новых видов лакокрасочных материалов.
Преимущества, которыми обладают лакокрасочные материалы (ЛКМ) на основе водных полимеров, способствуют ежегодному росту их производства и применения. На состоявшейся 3–4 декабря 2013 г. в г. Дюссельдорфе (Германия) конференции European Coatings Conference «Waterborne coatings» были рассмотрены достижения, проблемы и пути их решения в области водных ЛКМ.
Высокое качество водных 2К полиуретановых систем в сочетании с низкой эмиссией растворителей вызывает большой спрос промышленности.
Эти материалы успешно зарекомендовали себя во многих сегментах рынка, поскольку они позволяют преодолеть разрыв между растущей потребностью в «зеленых» решениях и требованиями к качеству со стороны промышленности и профессионалов.Поставщики лакокрасочных материалов (ЛКМ) постоянно совершенствуют качество водных систем, а сырьевая отрасль развивает инновационные концепции как для смол, так и для отвердителей.
В докладе д-ра Кристофа Ирла (Christoph Irle), Bayer Material Science (Германия), особое внимание было уделено производству и надежности таких составов. Рассмотрение этих вопросов в дальнейшем поможет получить водные 2К системы, близкие к самой высокой отметке, которая уже многие десятилетия установлена для 2К полиуретановых систем.
Продолжил тему полиуретанов д-р Норберт Питшман (Norbert Pietschmann), Institute fur Lack und Fabric (Германия), выступив с докладом «Водные УФ-отверждаемые ЛКМ для защиты стали от коррозии».
При испытаниях противокоррозионных свойств пигментов, ингибиторов, связующих или их комбинаций он использовал электрохимические измерения, обеспечивающие более быстрое получение результатов. Этим методом
было установлено, что оптимальная комбинация связующего состоит из смеси УФ-отверждаемых и физически высыхающих дисперсий.
Кроме того, был найден подходящий и быстрый способ выбора антикоррозионного пигмента и ингибитора. На основе предварительных исследований могут быть созданы модельные рецептуры с отличной адгезией и коррозионной стойкостью. После нанесения на сталь испарения влаги и УФ-отверждения были испытаны на стойкость к соляному туману и конденсации влаги.
Электрохимические исследования подтвердили отличную адгезию и устойчивость к коррозии, однако это было получено только на стальных поверхностях с цинкфосфатным подслоем.
Защита металла от коррозии в домашних условиях
Существуют ли «народные» средства против ржавчины?
И обычное железо, и даже высококачественная сталь во влажном воздухе, который наверняка присутствует в гаражах, сараях и прочих подсобных помещениях подвергаются коррозии — постепенно покрываются буро-коричневой рыхлой пленкой ржавчины.
Порой абсолютно новая вещь, случайно оставленная под открытым небом или «забытая» на зиму на даче, покрывается неприятной на вид бурой коростой.
Ржавчина, которая состоит из смеси оксида железа Fe2O3 и метагидроксида железа FeO(OH), не защищает его поверхность от дальнейшей «агрессии» со стороны кислорода воздуха и воды, и со временем некогда прочный железный предмет разрушается (очень часто полностью).
Секреты удаления ржавчины есть. Ржавчину проще всего снять обработкой разбавленным водным раствором соляной или серной кислоты, содержащим ингибитор кислотной коррозии уротропин.Ингибиторы (от латинского «ингибео» — останавливаю, сдерживаю) — вещества, тормозящие химическую реакцию (в данном случае реакцию растворения металла в кислоте).
Но ингибитор коррозии не мешает взаимодействию кислоты с оксидом и гидроксидом железа, из которых состоит ржавчина.
Если заржавели оконные шпингалеты, мелкие детали велосипеда, болты или гайки, их погружают в 5% раствор кислоты с добавкой 0,5 г уротропина на литр, а на крупные вещи такой раствор наносят кистью.
Использовать растворы сильных кислот без ингибитора рискованно: можно растворить не только ржавчину, но и само изделие, поскольку железо — активный металл и взаимодействует с сильными кислотами с выделением водорода и образованием солей.
В качестве ингибитора кислотной коррозии при удалении ржавчины можно использовать и картофельную ботву. Для этого в стеклянную банку кладут свежие или засушенные листья картофеля и заливают 5-7%-й серной или соляной кислотой так, чтобы уровень кислоты был выше примятой ботвы.
После 15-20-минутного перемешивания содержимого банки кислоту можно сливать и использовать для обработки ржавых железных изделий.
Преобразователь ржавчины превращает ее в прочное покрытие поверхности коричневого цвета. На изделие кистью или пульверизатором наносят 15-30%-й водный раствор ортофосфорной кислоты и дают изделию высохнуть на воздухе.
Еще лучше использовать ортофосфорную кислоту с добавками, например, 4 мл бутилового спирта или 15 г винной кислоты на 1 л раствора ортофосфорной кислоты. Ортофосфорная кислота переводит компоненты ржавчины в ортофосфат железа FePO4 , который создает на поверхности защитную пленку.
Одновременно винная кислота связывает часть производных железа в тартратные комплексы.
Металлические поверхности, сильно изъеденные ржавчиной, обрабатывают:
- смесью 50 г молочной кислоты и 100 мл вазелинового масла. Кислота превращает метагидроксид железа из ржавчины в растворимую в вазелиновом масле соль — лактат железа. Очищенную поверхность протирают тряпочкой, смоченной вазелиновым маслом;
- раствором 5 г хлорида цинка и 0,5 г гидротартрата калия в 100 мл воды. Хлорид цинка в водном растворе подвергается гидролизу и создает кислую среду. Метагидроксид железа растворяется за счет образования в кислой среде растворимых комплексов железа с тартрат-ионами;
Отворачивать приржавевшие гайки помогает смачивание керосином, скипидаром или олеиновой кислотой. Через некоторое время гайку удается отвернуть. Затем можно поджечь керосин или скипидар, которым ее смачивали. Обычно этого достаточно для разъединения гайки и болта.
Самый последний способ: к гайке прикладывают сильно нагретый паяльник.
Металл гайки расширяется, и ржавчина отстает от резьбы; теперь в зазор между болтом и гайкой можно впустить несколько капель керосина, скипидара или олеиновой кислоты, и на этот раз гайка отвернется ключом.
Есть и другой способ разъединения ржавых гайки и болта. Вокруг заржавевшей гайки делают «чашечку» из воска или пластилина, бортик которой выше уровня гайки на 3-4 мм. Заливают в чашечку разбавленную серную кислоту и кладут кусочек цинка. Через сутки гайка легко отвернется ключом.
Чашечка с кислотой и металлическим цинком на железном основании — это миниатюрный гальванический элемент.Кислота растворяет ржавчину, и образовавшиеся катионы железа восстанавливаются на поверхности цинка; в то же время металл гайки и болта не растворяется в кислоте до тех пор, пока у кислоты есть контакт с цинком, поскольку цинк более активный в химическом отношении металл, чем железо.
Чтобы предохранить от ржавления столярный или слесарный инструмент, его смазывают с помощью кисточки раствором 10 г воска в 20 мл бензина. Воск растворяют в бензине на водяной бане, не используя открытого огня (бензин огнеопасен).
Полированный инструмент защищают, нанося на его поверхность раствор 5 г парафина в 15 мл керосина.
А старинный рецепт мази для защиты металла от ржавчины таков: растапливают 100 г свиного жира, добавляют 1,5 г камфоры, снимают с расплава пену и смешивают его с графитом, растертым в порошок, чтобы состав стал черным. Остывшей мазью смазывают инструмент и оставляют его на сутки, а потом полируют металл шерстяной тряпочкой.
Чтобы в будущем не мучиться, отворачивая крепежные изделия с проржавевшей резьбой, ее заранее смазывают смесью вазелина с графитовым порошком. Вместо вазелина можно взять и любую другую жировую смазку нейтрального или слабощелочного типа. Болты и гайки на такой смазке легко отворачиваются даже через несколько лет пребывания под открытым небом.
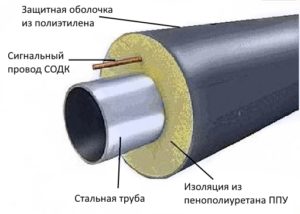
Защита металла в земле от коррозии
Коррозия — бич всех металлоконструкций, а протекающие трубы — страшный сон любого владельца жилья. Появление ржавчины неотвратимо, как смена времен года, ее вызывают физические и химические факторы окружающей среды. Но можно замедлить развитие коррозии и уменьшить ее разрушительное воздействие.
Металл и пластик: за и против
Расхожее мнение специалистов в области ремонта гласит, что есть только один радикальный способ борьбы с коррозией — замена всех труб на пластиковые.
Но металлические трубы так просто не сдаются, ведь не всегда есть возможность сделать капитальный ремонт во всей квартире. К тому же стальные и чугунные трубы гораздо прочнее и надежнее пластиковых и металлопластиковых.
Они более устойчивы к высокому давлению и температуре (особенно к их перепадам), имеют низкий коэффициент теплового расширения (не деформируются) и высокую теплопроводность.Пластик теоретически весьма долговечен, но это пока не проверено временем. Недостаточно изучена и безопасность этого материала при его длительном применении, но уже известно, что он боится хлорированной воды. Так что металлическим трубам все еще есть место в наших домах, а значит, проблема их защиты от коррозии по-прежнему актуальна.
Вокруг агрессия!
Как бороться с ржавчиной в бытовых условиях? Самый доступный способ — нанесение на металл средства, которое образует защитную пленку на его поверхности: краски, лака, эмали.
Лакокрасочные покрытия имеют низкую паро- и газопроницаемость и высокие водоотталкивающие свойства.
Таким образом, они не допускают к поверхности металла влагу, кислород и другие агрессивные вещества, которые и вызывают коррозию.
ЛКМ относительно недороги, легко наносятся обычной кистью или из спрея. Они сохраняют защитные свойства в течение нескольких лет. Их важное качество — устойчивость к высоким температурам, основной недостаток — чувствительность к механическим повреждениям и перепадам температуры, из-за чего на поверхности образуются мелкие трещины, открывающие доступ влаге и воздуху к металлу.
Поэтому окрашивание следует проводить регулярно.
Главное — качество!
Преграда в виде ЛКМ не останавливает коррозию полностью, а лишь замедляет ее. Поэтому на первый план выходит качество покрытия — высокая прочность сцепления состава с основанием (адгезия), равномерность нанесения, отсутствие пористости и воздушных пузырей. А качество покрытия напрямую связано с тем, как подготовлено основание.
Старая, отслаивающаяся краска должна быть тщательно удалена. Если труба ржавая, то нужно счистить рыхлые слои, а затем воспользоваться специальным преобразователем ржавчины (150-200 руб./кг). В основе таких средств — кислота (обычно ортофосфорная).
Она химически взаимодействует с ржавчиной и превращает ее в соли железа — нейтральное вещество, которое образует однородную и прочную дополнительную защитную пленку.
Защита металла от коррозии
Защита металла от коррозии выполняется при помощи всевозможных лакокрасочных составов и эмалей. В нашей статье вы найдёте характеристики наиболее популярных эмалей для защиты от ржавчины.
Такие эмали называются три в одном и пользуются большим спросом из-за того, что они помимо качественного красочного покрытия служат основой и защитой от ржавчины. Как утверждают производители, перед использованием краски не нужно счищать ржавчину.
Однако не спешите наносить краску на ржавчину, ведь непрочные ржавые частицы могут отвалиться после покраски.
Проведение тестирования
Мы купили следующие краски для защиты металла от коррозии:
- Снежка (Sniezka)
- Композит (Kompozit)
- Альпина (Alpina)
- Эмаль Текс
- Краска Зебра
Все краски зелёного цвета и могут использоваться прямо поверх ржавчины. Испытания проводились в лаборатории, проводящей испытания над изоляционными покрытиями от коррозии трубопроводов. Объекты тестировались по таким показателям:
- Процент нелетучих элементов. Такие элементы остаются после высыхания краски. Показатель вычисляется в процентном соотношении. То есть чем выше будет число, тем более толстый слой краски получится. А значит, защита металла будет выше.
- Скорость высыхания. От этого показателя зависит быстрота нанесения последующего слоя и период, когда можно начинать эксплуатировать покрашенный объект. В лаборатории испытывали объекты до третьей стадии просыхания. Кстати, обычно период, через который можно наносить последующий слой, меньше, чем сроки полного просыхания.
- Сцепление с основой. Чем лучше эмаль сцепится с верхним слоем окрашиваемого объекта, тем надёжнее она будет держаться.
- Прочность высохшего слоя. Чем крепче будет слой, тем прочнее и долговечнее будет покрытие.
Тестирование проводилось согласно ГОСТ. А значит, защита металла от коррозии при помощи краски должна быть самой оптимальной. Помимо проведения лабораторных исследований краску подвергли органо-лептическому изучению.
Для точности опытов вся химия, с помощью которой проводится защита металлов от коррозии, наносилась на ржавую предварительно очищенную основу.
Все работы были выполнены в ясную погоду при температуре воздуха не ниже двадцати градусов.
Во время окраски проводилась оценка лёгкости нанесения состава, а также качества полученного покрытия (подтёки, морщины, расслоения). Помимо этого, в ходе исследований проводился подсчёт расхода краски.Это было нужно для того, чтобы потом сравнить полученный показатель с данными, указанными на банке.
Все результаты мы предоставим в форме таблицы «Защита металлов от коррозии лакокрасочными покрытиями: сравнение».
Лучшая защита металла от коррозии: результаты лабораторных анализов
Кроме данных из таблицы оценки красок, с помощью которых выполняется защита металлов и сплавов от коррозии, стоит учесть и такие моменты:
- Упаковка. Внешне все производители использовали качественные упаковки и снабдили их всей необходимой информацией о содержимом банки. Однако при внешнем сходстве габаритов банок, их объём может немного отличаться. Так, производители краски Sniezka для защиты металлов от коррозии используют банки объёмом 650 мл. А производители Зебра и Альпина выбрали банки объёмом 750 м л. Средства защиты металла от коррозии марки Kompozit и Текс продаются весом по 0,9 кг. Если учесть плотность краски, то получится что меньший объём у краски Снежка, а самый наибольший у Текс.
- Открывание банки. Все банки открывались обычной отвёрткой. Проблемы возникли, только с тарой производителя Зебра. В данных банках использовалась нетиповой зажим крышки, что может вылиться в дальнейшие неудобства в ходе эксплуатации.
- Нанесение краски. Обычно защита металла от коррозии при помощи краски в домашних условиях выполняется при помощи кисти, поэтому и мы использовали этот инструмент. Все образцы красок легко наносились, без образования неровностей и потёков. Единственный состав, с нанесением которого возникли проблемы, – это Зебра. Химическая защита металлов от коррозии при помощи этого состава будет некачественной из-за низкой вязкости краски. Яркость краски у данного производителя самая невысокая. Равномерность слоя у Зебры также была хуже всего, зато наилучший результат показали Текс и Alpina.
- Запах от состава. Если защита металла от коррозии при помощи краски выполняется по СНИП, то допускается определённый запах от состава. Именно такой запах был у тестируемых образцов. Однако состав Kompozit имеет наиболее резкий запах уайт-спирита. Это связано с тем, что данная краска имеет самый большой объём нелетучих веществ. А состав марки Alpina, наоборот, был практически без запаха.
- Полное время высыхания. Данный показатель был на высоте у всех производителей. Через полчаса наблюдалось полное высыхание первого слоя. Основы коррозии и защиты металлов гласят, что для большего результата лучше использовать несколько слоёв лакокрасочного покрытия. Однако, скорее всего, такая скорость высыхания была связана с жаркой летней погодой. На банках разных производителей были указаны другие данные. Так, Sniezka должна высохнуть за 40 минут, Kompozit – за 90 минут, Alpina – 2-3 часа, Текс – 5-7 часов, Зебра – 8 часов.
- Расход. Эту проверку проводили методом проверки объёма с дальнейшей окраской гладкого стального листа площадью один квадратный метр. После этого проводились измерения оставшегося объёма краски. Затем разница между показателем объёма до начала работ и после него делится на площадь листа. Коррозия металлов предусматривает различные методы защиты от неё, но покраска – наиболее доступный. В ходе испытаний производилась окраска металлического листа при температуре не ниже 20 градусов. В итоге можно сказать, что наилучший результат у краски Текс, а самый худший у Kompozit. Поэтому если вы хотите купить экономичный состав, то лучшая защита металла от коррозии – Текс. Однако хоть показатели у всех составов различаются, они укладываются в допустимые рамки.
Почвенная коррозия
Почвенная коррозия – разрушение металла в почве. Ежегодные потери металла вследствии протекания почвенной коррозии достигают 4%.
Почвенной коррозии подвергаются различного назначения трубопроводы, резервуары, сваи, опоры, кабеля, обсадные трубы скважин, всякого рода металлоконструкции, эксплуатируемые в почве.
Почва – очень агрессивная среда. Она состоит из множества химических соединений и элементов, многие из них только ускоряют коррозионный процесс. Агрессивность почвы (грунта) зависит от некоторых факторов: влажность, аэрация, пористость, рН, наличие растворенных солей, электропроводность.
Классификация грунтов по коррозионной активности:
— высококоррозионные грунты (тяжелые глинистые, которые длительное время удерживают влагу);
— среднекоррозионные грунты;
— практически инертные грунты в коррозионном отношении (песчаные почвы).
Влияние влажности грунта на почвенную коррозию металла
Влага в почве присутствует почти везде. Где-то ее больше, а где-то меньше. Именно влажность грунта очень сильно влияет на скорость почвенной коррозии, превращая почву в электролит. Она же вызывает электрохимическую коррозию находящихся в грунте металлоконструкций.
Вода в грунте может быть: капиллярной, гравитационной, связанной. Капиллярная влага собирается в порах грунта. Высота подъема ее по капилляру зависит от диаметра пор. Капиллярная влага сильно влияет на скорость почвенной коррозии.
Связанная влага на скорость почвенной коррозии не влияет, т.к. находится в виде гидратированных химических соединений.
Под действием силы тяжести в грунтах и почвах постоянно перемещается вода, которая оказывает, как и капиллярная, значительное влияние на скорость почвенной коррозии.
Максимальная скорость почвенной коррозии наблюдается при влажности грунта 15 – 25%. Это объясняется уменьшением омического сопротивления коррозионных элементов.
С повышением влажности почвы анодный процесс проходит легче (за счет затруднения пассивации поверхности металла), а катодный – труднее (грунт насыщается влагой, затрудняется его аэрация).
Влажность, при которой наблюдается наибольшая скорость коррозии, называют критическим показателем влаги для грунта. Для глинистых грунтов он составляет около 12 – 25%, для песчаных 10 – 20%.
Пористость (воздухопроницаемость) грунта
Пористость (воздухопроницаемость) грунта влияет на способность длительное время сохранять влагу и аэрацию. Воздухопроницаемость зависит от состава грунта, его плотности, влажности.
Грунты, хорошо пропускающие воздух (песчаные), более агрессивны. В песчаных грунтах катодный процесс протекает с облегчением.
На практике бывают случаи, когда подземный трубопровод большой протяженности проходит через разного вида грунты.
Если он проходит последовательно в песчаной, а потом глинистой почве, где условия аэрации металлической поверхности очень различаются, то возникают аэрационные микрогальванические коррозионные зоны.Поверхность трубопровода в песчаной зоне будет играть роль катода, а глинистой – анода. Разрушение металла будет происходить на анодных участках, где затруднен доступ кислорода к поверхности. Интересно, что катодная и анодная зоны могут находится на расстоянии больше сотни метров.
При этом коррозионный процесс будет отличаться омическим торможением.
Кислотность грунта
Для большинства грунтов значение рН составляет 6,0 – 7,5. Высококоррозионными являются почвы, рН которых сильно отличается от данного значения.
К ним относятся торфяные, болотистые грунты, значение рН которых составляет 3 – 6. А также щелочные солончаки и суглинки, с рН почвы 7,5 – 9,5.
Очень агрессивной средой по отношению к сталям, свинцу, меди, цинку является чернозем, содержащий органические кислоты.
Одна из самых агрессивных почв – подзол. Сталь в подзоле корродирует в 5 раз быстрее, чем в других грунтах.
Кислотность грунтов ускоряет почвенную коррозию, т.к. вторичные продукты коррозии становятся более растворимы, существует возможность дополнительной катодной деполяризации ионами водорода.
Электропроводность грунта
Электропроводность грунта зависит от его минералогического состава, количества влаги и солей в почве. Каждый вид грунта имеет свое определенное значение электропроводности, оно может колебаться от нескольких единиц до нескольких сотен Ом на метр.
Соленость грунта оказывает огромное влияние на его электропроводность. С увеличением содержания солей легче протекают анодный и катодный электродные процессы, что снижает электросопротивление.
Почти всегда определив электропроводность грунта можно судить о его степени коррозионной агрессивности (для стали, чугуна). Исключение составляют водонасыщенные почвы.
Минералогический состав и неоднородность грунта
Минералогический состав и неоднородность грунта оказывают большое влияние (как и влажность) на омическое сопротивление. В глинисто-песчаном влажном грунте удельное сопротивление почвы составляет около 900 Ом•см, а в таком же грунте, только сухом – 240000 Ом•см. С уменьшением удельного сопротивления грунта его агрессивность увеличивается.
Минерализация почвы может колебаться в пределах 10 – 300 мг/л.
Неоднородность грунта приводит к возникновению гальванопар, которые только усиливают почвенную коррозию, делают разрушение неравномерным.
Влияние температуры грунта на почвенную коррозию металлов. Температура может колебаться в очень больших пределах. Зимой, когда свободная вода, заполняющая капилляры в почве замерзает — скорость почвенной коррозии немного уменьшается. Это также связано с плохой аэрацией поверхности металла.
В летнее время, когда на улице стоит жара, скорость почвенной коррозии может замедлятся также, что объясняется высыханием почвы. Самый большой ущерб почвенная коррозия наносит в межсезонье, когда грунт достаточно влажный, созданы оптимальные условия для протекания коррозионного процесса.Температура грунта зависит от времени года, географической широты, времени суток, погоды.
Значительное различие температур на конструкции, имеющей большую протяженность (подземный трубопровод) может быть причиной образования термогальванических коррозионных пар, которые обеспечивают усиление местной почвенной коррозии.
Влияние микроорганизмов на почвенную коррозию металлов
В почве живут и развиваются два вида микроорганизмов: аэробные (могут существовать только при наличии кислорода), анаэробные (для обеспечения их жизнедеятельности кислород не требуется).
Они оказывают огромное влияние на почвенную коррозию металлов.
Почвенная коррозия металлических сооружений, вызванная жизнедеятельностью живых микроорганизмов носит название биологическая (биокоррозия) либо биохимическая.
Аэробные микроорганизмы (почвенные) существуют двух видов: одни принимают непосредственное участие в осаждении железа, другие – окисляют серу. Оптимальными условиями для существования анаэробных серобактерий является кислая среда (3 – 6 рН). Серобактерии окисляют сероводород в серу, а потом — серную кислоту по следующим уравнениям:
2H2S + O2 = 2H2O + S2;
S2 + 2H2O + 3O2 = 2H2SO4.
В местах наибольшего количества серобактерий концентрация серной кислоты может достигать 10%. Это очень сильно ускоряет почвенную коррозию, особенно стали.
При рН грунта около 4 – 10 развиваются бактерии, перерабатывающие железо. Эти бактерии в процессе своей жизнедеятельности поглощают ионы железа, а выделяют нерастворимые соединения, содержащие Fe.
В местах скопления железобактерий наблюдается большое количество нерастворимых железистых соединений, которые увеличивают гетерогенность поверхности.
Это явление также оказывает большое влияние на скорость почвенной коррозии.
Анаэробные микроорганизмы могут вырабатывать углеводороды, сероводород, угольную кислоту и множество других химических соединений. Они могут разрушать защитные покрытия, воздействовать на ход анодной и катодной реакции, менять характеристики почвы.
Среди анаэробных микроорганизмов самыми опасными можно считать сульфатредуцирующие бактерии. Оптимальные условия для их существования, почва со значением рН 5,5 – 8 (болотные, глинистые, илистые грунты). Бактерии восстанавливают сульфаты, содержащиеся в почве. Этот процесс можно описать следующим уравнением:MgSO4 + 4H = Mg(OH)2 + H2S + O2.
Выделившийся кислород обеспечивает протекание реакции на катоде. Сероводород и сульфиды в почве являются причиной появления на поверхности эксплуатируемой конструкции рыхлого слоя сульфида железа.
Коррозия носит питтинговый характер.
Механизм и особенности почвенной коррозии металлов
Почвенная коррозия почти всегда протекает по электрохимическому механизму (исключения составляют лишь очень сухие грунты).
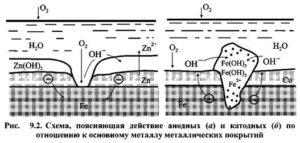
Анодный процесс при почвенной коррозии – разрушение металла. На катоде же проходит кислородная деполяризация.
Чаще всего кислородная деполяризация проходит с затрудненным доступом кислорода к поверхности корродирующего изделия.
Подвод кислорода может осуществятся несколькими способами: диффузией в жидкой или газообразной среде или направленным течением этих фаз, перемешиванием фаз при помощи конвекции.
Во влажном грунте процесс проходит с преимущественно катодным контролем, а сухих рыхлых почвах — анодным. Иногда, при работе протяженных микропар может наблюдаться катодно-омический контроль.
На катоде также может проходить и водородная деполяризация (только в условиях кислых грунтов). Существенно изменить ход коррозионного процесса могут и микроорганизмы.
Подземную коррозию делят на грунтовую коррозию и электрокоррозию (коррозию блуждающими токами). Подземная коррозия менее опасна, чем разрушение под воздействием блуждающих токов.
Особенности почвенной коррозии металлов:
— значительное влияние омического сопротивления грунта;
— возникновение коррозионных микро и макропар;
— язвенный характер разрушения.
Методы защиты от почвенной коррозии
Защиту от почвенной коррозии можно разделить на активную (электрохимическую) и пассивную (изоляция изделия от воздействия окружающей среды, специальные способы укладки и т.д.).
Для защиты металлоизделий от почвенной коррозии применяются самые разнообразные методы. Очень часто, особенно в высококоррозионых грунтах, применяют комплексную защиту от подземной коррозии.
Основные методы защиты металлоконструкций от почвенной коррозии: нанесение защитных покрытий и изоляция изделий, создание искусственной среды, электрохимическая защита, применение специальных методов укладки.
Нанесение защитных покрытий. Изоляция
Для защиты от почвенной (грунтовой) коррозии наиболее эффективным и широко используемым является нанесение защитных изоляционных покрытий.
К таким покрытиям предъявляются следующие требования: оно должно быть сплошным, без трещин, царапин; иметь хорошую адгезию с металлоподложкой; быть химически стойким; отличаться высокими диэлектрическими свойствами; сохранять свои защитные свойства при воздействии положительных и отрицательных температур (от -50 до +50 °С); не содержать коррозионно-активных по отношению к основному металлу агентов; обладать высокой биостойкостью, механической прочностью.
Защитные покрытия могут быть полимерными и мастичные. К мастичным относятся каменноугольное, битумное. К полимерным – покрытия из липких изоляционных лент, расплавы, накатываемые эмали и т.д.
Покрытие, применяемое для защиты от почвенной коррозии, должно полностью изолировать готовую конструкцию от воздействия окружающей среды. Для изоляции подземных трубопроводов очень часто используют битумные покрытия различной толщины (6 мм – усиленное, 3 мм – обычное, 9 мм – очень усиленное).Широкое распространение получили петролатумные, цементные, каменноугольно-пековые, полиэтиленовые, поливинилхлоридные защитные покрытия. Последние отличаются отличными защитными и изолирующими способностями, долгим сроком службы, но не из самых дешевых.
Самыми слабыми защитными свойствами обладает цементное покрытие.
Создание искусственной атмосферы
Этот метод применяют достаточно редко, в основном для трубопроводов большой протяженности. Это связано с большими транспортными затратами, трудностью его реализации (необходимо большое количество работников, техники, достаточно много времени).
Протяженные подземные сооружения могут проходит через разные виды почв, что интенсифицирует коррозионный процесс. Суть метода заключается в том, чтоб создать однородный грунт по всей протяженности конструкции (засыпая, например, весь трубопровод песчаным грунтом) либо уменьшить агрессивность почвы на определенных участках. Для этого кислые грунты могут известковать.
Электрохимическая защита металла от почвенной коррозии
Электрохимическая защита заключается в принудительном создании катодной либо анодной поляризации. При совместном применении электрохимический защиты и защитных покрытий, затраты на первую весьма невелики.
В практике защиты металлов от почвенной коррозии очень часто применяется катодная защита. Металлоконструкции сообщают определенный отрицательный электрический потенциал, который затрудняет термодинамику окисления металла. Это существенно снижает (сводит к минимуму) скорость почвенной коррозии. Осуществить катодную поляризацию можно используя специальные установки: протекторные, катодные.
Протекторная защита заключается в подсоединении к изделию электродов из металла, который в данной среде более электроотрицателен. Для защиты стали от подземной коррозии протекторами могут служить алюминий, его сплавы, цинк, магний.
Катодная защита – создание катодной поляризации при помощи внешнего источника тока (генераторы постоянного тока, батареи, выпрямители). По всей протяженности трубопровода ставят специальные станции катодной защиты.
Специальные методы укладки
Очень часто при прокладке трубопровода, а также других сооружений для защиты их от воздействия грунтовых вод, самого грунта используют специальные способы укладки. Трубопровод или кабель может быть помещен в специальный коллектор (при этом кабель укладывают на неметаллическую подкладку), защитный кожух (часто из железобетонных плит или металла).
Вышеописанные методы применимы только для защиты изделий от влияния грунта и подземных вод.